時間:

作者:梁苑英竹,袁松、郭寧子等
目的:研究注射用醋酸奧曲肽微球體外釋放度加速試驗(yàn)方法,并探討與體內(nèi)釋放的相關(guān)性,為該制劑 的有效性評價研究提供參考。方法:分別采用轉(zhuǎn)瓶法和流池法考察了溫度、pH、轉(zhuǎn)速、流速、樣品池的種類、膜的排列方式、玻璃珠以及加樣方式等影響因素,建立了體外加速釋放在溫度 37 ℃、片劑池(22.6 mm)、流 速 16 mL ·min-1 和 pH 10.0 緩沖液中進(jìn)行的流池法,并與在溫度 37 ℃、轉(zhuǎn)速6r ·min-1 和 pH 10.0 緩沖液中進(jìn)行的轉(zhuǎn)瓶法進(jìn)行對比。結(jié)果:注射用醋酸奧曲肽微球在流池法中的釋放均快于轉(zhuǎn)瓶法中的釋放;且2種制劑樣品不同方法測定結(jié)果趨勢一致,制劑A釋放快于制劑B;對流池法體外加速釋放 - 體內(nèi)釋放進(jìn)行線性回歸,制劑A和B相關(guān)系數(shù)r分別為0.998 2、0.960 9 。結(jié)論:采用流池法測定的體外加速釋放快于轉(zhuǎn)瓶法,且與體內(nèi)釋放具有良好的相關(guān)性(r>0.9),為評價奧曲肽微球制劑的體內(nèi)外釋放提供參考。

注射用醋酸奧曲肽微球臨床主要用于治療肢端肥大癥等疾病,肌肉注射給藥,給藥周期為28d。該微球制劑由諾華制藥原研,于2003年在我國獲批上市,目前國內(nèi)尚未有仿制制劑上市。奧曲肽微球在處方和工藝上均與亮丙瑞林等其他多肽微球注射劑不同,采用葡萄糖星型丙交酯和乙交酯共聚物作為生物可降解緩釋輔料,采用相分離法制備微球,其質(zhì)量控制與藥學(xué)評價技術(shù)方法面臨挑戰(zhàn)。釋放度是評價緩釋微球制劑的關(guān)鍵質(zhì)量指標(biāo),體外釋放試驗(yàn)一般分為突釋釋放、加速釋放和常速釋放。針對注射用醋酸奧曲肽微球的體外釋放度,F(xiàn)DA溶出度數(shù)據(jù)庫推薦采用流池法、槳法等裝置進(jìn)行研究;文獻(xiàn)建立了常速釋放轉(zhuǎn)瓶測定法,試驗(yàn)周期為 36d,重 點(diǎn)對突釋階段進(jìn)行了研究;尚未見體外加速試驗(yàn)方面的研究報道。為提高注射用微球制劑質(zhì)量監(jiān)測與評價的效率,有必要對該制劑的體外加速釋放度試驗(yàn)方法進(jìn)行研究。
文獻(xiàn)報道注射用微球制劑的體外釋放度方法有直接釋藥法、透析膜擴(kuò)散法、流池法等,各有特點(diǎn)。采用水浴轉(zhuǎn)瓶裝置的直接釋藥法,雖然操作簡便,但微球易聚集或浮動,且在進(jìn)行分離時樣品容易損失,對最終試驗(yàn)結(jié)果產(chǎn)生影響。流池法即美國藥典溶出度測定第Ⅳ法,包括開環(huán)和閉環(huán)2 種模式,將微球置于樣品池中,釋放介質(zhì)往復(fù)通過樣品池中的微球,定時取樣并補(bǔ)充相應(yīng)的釋放介質(zhì)。此方法因能更好的模擬人體內(nèi)環(huán)境,生物相關(guān)性良好,被美國FDA推薦作為測定PLGA微球釋放度的最適方法,但其成本過高,且存在反壓力和過濾器堵塞的風(fēng)險。
本文通過考察溫度、流速、pH、樣品池、樣品裝填方式等條件,建立了流池法測定注射用醋酸奧曲肽微球體外加速釋放度,并與轉(zhuǎn)瓶法進(jìn)行對比研究,同時采用LC-MS法測定大鼠血漿中奧曲肽的濃度,探討分析體外加速釋放和體內(nèi)釋放行為,為醋酸奧曲肽微球注射劑的有效性評價研究提供參考。
2.1儀器與試藥
儀器:Agilent1260高效液相色譜儀、Agilent1290高效液相色譜(Agilent 公司);QTRAP 5500MS/MS系統(tǒng)(Agilent 公司);轉(zhuǎn)瓶裝置(Rotating Bottle Apparatus,Agilent 公司);流通池(推薦使用華溶DS-7CP流池法溶出系統(tǒng));真空脫氣儀(推薦使用華溶DGU-900在線溶媒脫氣機(jī));Fresco21 XIR臺式離心機(jī)(ThermoHeraeus 公 司);VORTEX 多功能漩渦混合器(Scientific公司); Turbo Vap 蒸發(fā)儀(Biotage 公司)。
試藥:醋酸奧曲肽對照品(批號140730-201303,含量87.6%,中國食品藥品檢定研究院);13C6-Lys Octreotide Tri(TRC 公司);注射用醋酸奧曲肽微球和溶 媒樣品(生產(chǎn)企業(yè) A、生產(chǎn)企業(yè) B);濾膜(GF/F:0.7 μm,批號 9565828,GF/D:2.7 μm,批號 9739611,Whatman 公司);濾頭(2μm;Upchurch公司);固相萃取柱(Oasis WCX 1 cc/30 mg,30μm,WATERS OASIS 公司)。
試劑:甲醇(批號SB6SF66072;MERCK 公司)、 甲酸(批號402907,F(xiàn)LUKA 公司); 丙酸(批號SHBC7498V,F(xiàn)LUKA公司);磷酸(≥ 85.0%)、冰醋酸(≥99.5%)、三水乙酸鈉(≥99.0%)、氯化鈉 (≥99.5%)、氯化銨(≥99.5%)均來源國藥集團(tuán)化學(xué)試劑有限公司;四甲基氫氧化銨五水合物(97%,北京百靈威科技有限公司);乙腈(99%,F(xiàn)isher Scientific 公司);十二烷基硫酸鈉(批號100809-201302,≥ 95%,中國食品藥品檢定研究院)。
2.2 體外釋放度測定——轉(zhuǎn)瓶法
緩沖液(pH4.0):稱取0.9g冰醋酸,用250mL水溶解,用5mol ·L-1氫氧化鈉溶液調(diào)節(jié)pH4.0。加入5.25g十二烷基硫酸鈉,慢慢攪拌使溶解。緩沖液(pH7.0):稱取 1.35 g 氯化銨至250mL量瓶,用水溶解后用三乙胺調(diào)節(jié)pH為7.0±0.1。 加入5.25g十二烷基硫酸鈉,慢慢攪拌使溶解。緩沖液(pH10):稱取2.7g氯化銨至500 mL 量瓶,用450mL水溶解,量取6.0mL三乙胺加入瓶中,混勻,用水定容至刻度。用三乙胺調(diào)節(jié)pH為10.0±0.1,加入10.5 g十二烷基硫酸鈉,慢慢攪拌使溶解。
供試品溶液:取適量微球,置40mL 轉(zhuǎn)瓶中,加入30mL 緩沖液,擰緊瓶蓋,立即將轉(zhuǎn)瓶與裝置連接并開始旋轉(zhuǎn)。在1、4、24h 從裝置上移除轉(zhuǎn)瓶,取出500μL,過濾,將300μL 濾液倒回轉(zhuǎn)瓶中,將剩下的200 μL濾液置于自動進(jìn)樣瓶中。
2.2.2實(shí)驗(yàn)裝置
水浴轉(zhuǎn)瓶裝置(Rotating Bottle Apparatus,Agilent 公司)。
2.3 體外釋放度測定——流池法
2.3.1 試液配制
緩沖液(pH 4、7、10):同“2.2”項(xiàng)下方法。
供試品溶液:取適量微球,置樣品池中,加入60mL 緩沖液于瓶中。在 1、4、8、12、24、36、48h時取 出500μL 等分部分,過濾,將300μL濾液倒回瓶中, 將剩下的200μL 濾液置于自動進(jìn)樣瓶中。
2.3.2 實(shí)驗(yàn)裝置
采用美國藥典溶出度測定第Ⅳ 法 - 流池法裝置。
2.4 HPLC 條件
色譜柱:Brownlee NEW GUARD,RP-18,Aquapor,(7 μm,3 mm×15mm),Brownlee Spheri-5,RP-18(5 μm,4.6 mm×100mm );流動相:水-乙腈 - 四甲基氫 氧化銨溶液(1200 ∶600 ∶200 );流速:1.2mL ·min-1;檢測器DAD;檢測波長:210nm;柱溫:室溫;進(jìn)樣器溫度: 8 ℃; 進(jìn)樣體積:10μL;等度洗脫。
2.5 體內(nèi)釋放測定
2.5.1 動物實(shí)驗(yàn)
供試品溶液制備:分別精密稱取微球樣品(生產(chǎn)廠A和B)適量,加入溶媒5mL,配制成質(zhì)量濃度約為2mg ·mL-1混懸液。
動物與給藥:取18只雄性成年鼠,體重為200~ 250g,均分為3 組,分別為A 組、B組、空白組,每組6只。按給藥體積為1.0 mL ·kg-1,對A組、B組分別肌肉注射給藥樣品 A、B混懸液,各組應(yīng)在5min之內(nèi)完成給藥,避免懸浮液中沉淀生成。
樣品的采集與儲存:于 0、0.25、0.5、1、2、6 h 和 1、2、3、4、7、9、11、13、15、18、21、25、28、32、35、42、 49、56 d 從 SD 大鼠的眼眶后靜脈叢采血0.5mL,將血液加入預(yù)置5μL濃度為50 TIU ·mL-1的抑肽酶和5μL肝素的抗吸附EP管中(冰盒上),混勻。4℃下,12000r ·min-1離心10min,取上清液至另一抗吸 附EP管中,-80℃保存待測。
2.5.2 樣品前處理
精密移取大鼠空白血漿100μL,加稀釋液(甲醇-水-甲酸(60∶40∶0.2 )100μL,內(nèi)標(biāo)(13C 6Octretide 20 ng ·mL-1 )100μL,于1.5mL 離心管中,加入4% 磷酸水溶液100 μL,混勻;活化固相萃取柱;將樣品加于固相萃取柱中后離心,先后加洗滌液,離心洗去雜質(zhì),再加入洗脫液洗脫樣品,離心( 1 000 r ·min-1,2 min )用玻璃管收集洗脫液;洗脫液 置于50 ℃水浴,N2吹干后,用100μL稀釋液溶解后進(jìn)樣至液相色譜質(zhì)譜儀。
2.5.3 LC-MS 分析法
色譜條件:色譜柱Eclipse plus RRHD C18(50mm×2.1mm,1.8 μm ),流動相甲醇(A )-0.02% 丙酸水溶液(B),流速0.5mL ·min-1,柱溫 45℃,進(jìn)樣體積10μL,梯度洗脫(見表 1)。
表 1 梯度洗脫程序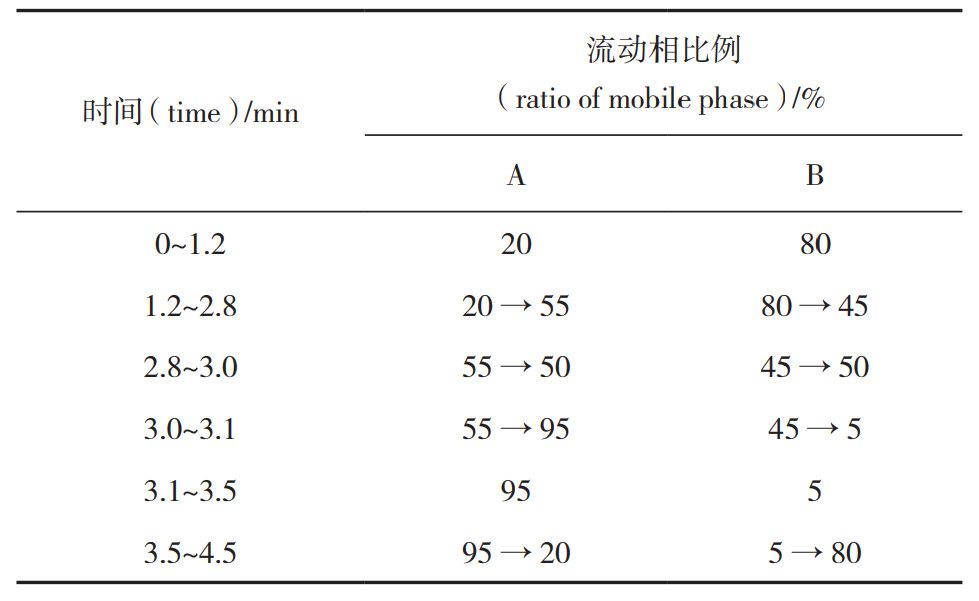
質(zhì)譜條件:離子源,電噴霧離子化源,正電子方式檢測;溫度 500 ℃ ; 氣簾氣體(CUR,N2 )壓力0.2MPa;離子噴射電壓 5000 V;源內(nèi)氣體1(GS1,N2 )壓力0.4 MPa;源內(nèi)氣體 1( GS2 ,N2)壓力0.4 MPa;掃描方式,多反應(yīng)監(jiān)測(MRM );奧曲肽m/z 510.4>120.1;去簇電壓(DP)120V;碰撞能量(CE),25 V;內(nèi)標(biāo)13C6Octretidem/z513.5>120.1;去簇電壓 (DP)100 V;碰撞能量(CE):25V
3.1體外加速釋放實(shí)驗(yàn)影響因素考察
3.1.1 轉(zhuǎn)瓶實(shí)驗(yàn)法影響因素
轉(zhuǎn)瓶法實(shí)驗(yàn)按照表2設(shè)計(jì)進(jìn)行,實(shí)驗(yàn)因素考察結(jié)果見圖1。溫度:如圖1-a所示,4h內(nèi)微球在45℃、55 ℃條件下釋放較慢,推測是由于高溫使聚合物 PLGA 發(fā)生形態(tài)變化,閉合了表面孔隙從而減少了藥物的擴(kuò)散;4h后在 55 ℃時條件下微球中藥物釋放突增,推測是由于更高的溫度加快了聚合物的溶蝕作用,這與文獻(xiàn)報道相一致; 在37℃下釋放平穩(wěn)且24h釋放量超過 60%。綜合考慮,最終選擇37℃作為體外加速釋放試驗(yàn)的溫度。
轉(zhuǎn)速:由圖1-b可見,轉(zhuǎn)瓶法轉(zhuǎn)速24 r ·min-1以 內(nèi),轉(zhuǎn)速增加釋放增多,轉(zhuǎn)速超過24r ·min-1釋放并未繼續(xù)增加。
釋放介質(zhì):如圖1-c所示,pH 4.0、pH 7.0 條件下24h內(nèi)基本不釋放,pH10條件下24h內(nèi)釋放量超過60%。根據(jù)酸堿催化理論,大量的氫離子或氫氧根離子都會誘導(dǎo) PLGA 內(nèi)酯鍵裂解,從而達(dá)到加速釋放的目的。
轉(zhuǎn)瓶法體外加速釋放條件最后選擇為溫度37℃、轉(zhuǎn)速 6 r·min-1、pH10 釋放介質(zhì)。
表 2 轉(zhuǎn)瓶法實(shí)驗(yàn)條件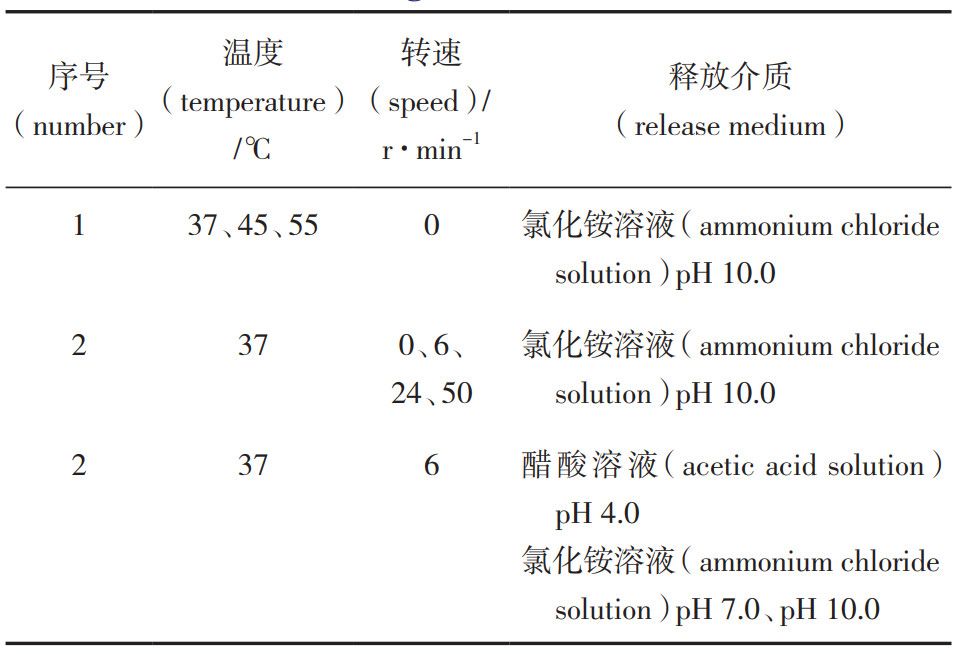
3.1.2 流通池實(shí)驗(yàn)法影響因素
在轉(zhuǎn)瓶法實(shí)驗(yàn)條件基礎(chǔ)上,利用流通池對玻璃珠及樣品裝填方式、粉體池濾膜、樣品池、樣品濃度、流速等條件進(jìn)行考察,實(shí)驗(yàn)按照表3設(shè)計(jì)進(jìn)行。
圖 1 不同影響因素的釋放度曲線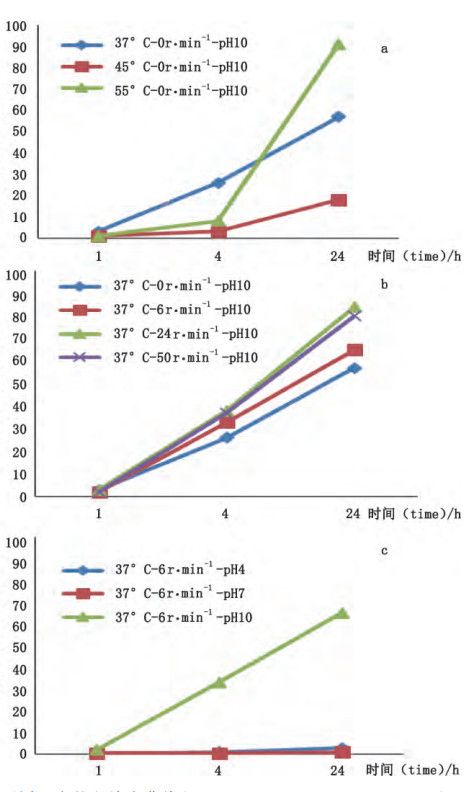
a. 不同溫度的釋放度曲線
b. 不同轉(zhuǎn)速的釋放度曲線
c. 不同緩 沖液的釋放度曲線
樣品量:由圖2-a 可見,含 3.10 mg ·mL-1 奧曲肽的混懸液釋放最快。
玻璃珠體積及樣品裝填方式:由圖 2-b 可見,玻璃珠體積、溶媒的加入對微球釋放的影響較小,加樣前后均加入玻璃珠釋放較快。
粉體池中過濾膜:膜的典型排列方式如圖3,由圖2-c結(jié)果可見,膜的排列方式對釋放的影響不大。
樣品池:由圖2-d可見,使用片劑大池(22.6 mm )、片劑小池(12 mm)、粉體池的釋放度依次遞減,這可能是由于片劑小池(12 mm)和粉體池的體積較小,微球中PLGA溶脹后易堵住過濾器而造成的。
流速:從圖2-e 可知,流速增加釋放度增大。
表 3 流池法實(shí)驗(yàn)條件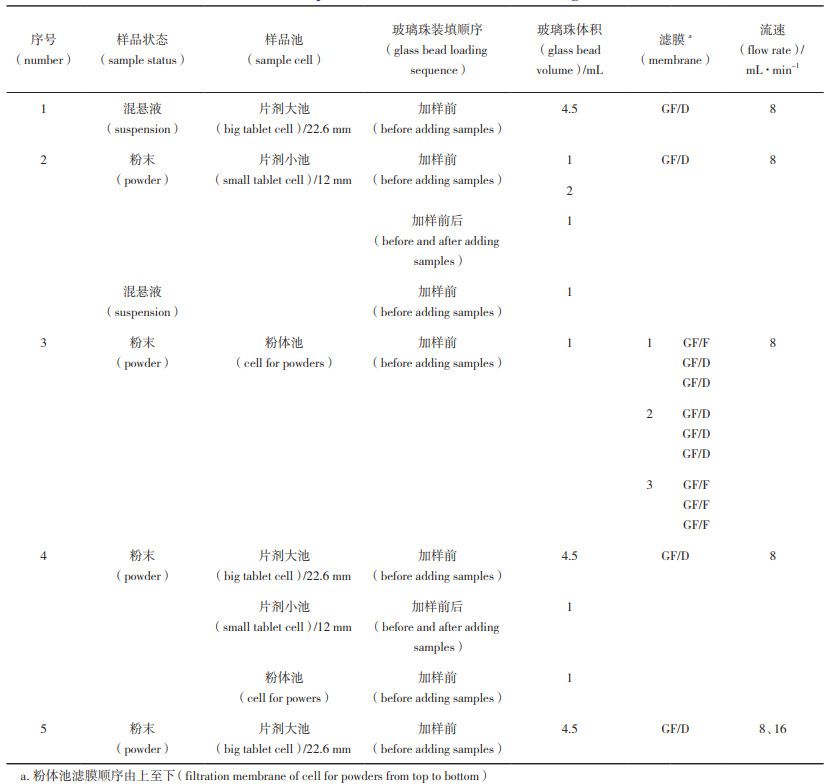
流池法最后選擇的條件為溫度37 ℃、片劑大池、流速16 mL ·min-1、pH 10釋放介質(zhì)。
3.2 體外加速釋放度測定
本研究通過改變溫度、pH、轉(zhuǎn)速/流速等條件加 速了藥物從PLGA微球中釋放,最終建立了流池法體外加速釋放測定方法,分別測定不同企業(yè)微球樣品,并與轉(zhuǎn)瓶法結(jié)果進(jìn)行對比。由表4 可見,2種方法測定的體外加速釋放度,4h后樣品A的釋放度均大于 樣品B,且采用流池法測定體外釋放度,樣品A和B的釋放度均明顯大于轉(zhuǎn)瓶法。
3.3 體內(nèi)釋放測定
微球經(jīng)皮下或肌肉注射給藥后,藥物從微球中釋放后通過皮下或骨骼肌的結(jié)締組織擴(kuò)散,再經(jīng)毛細(xì)血管吸收進(jìn)入血液循環(huán)分布到靶器官發(fā)揮藥效。本文利用大鼠對2家企業(yè)的醋酸奧曲肽微球 進(jìn)行體內(nèi)釋放試驗(yàn),通過LC-MS 檢測大鼠體內(nèi)奧曲 肽血藥濃度,研究該微球制劑藥物的體內(nèi)釋放行為。 A、B 2 組大鼠血漿中奧曲肽濃度測定結(jié)果見圖 4。
圖 2 流池法釋放曲線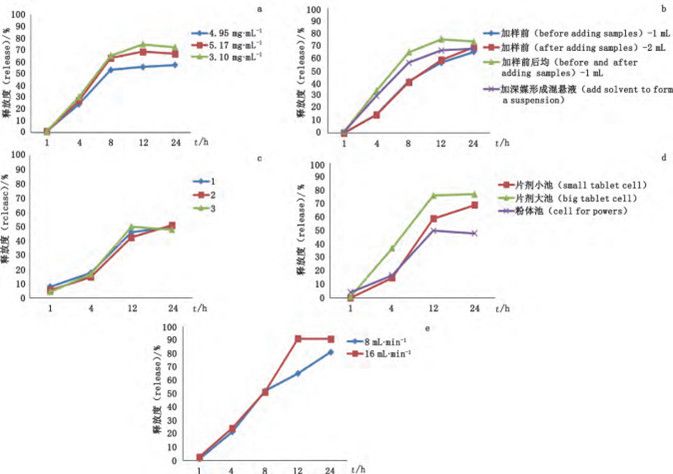
a. 不同濃度
b. 不同玻璃珠體積及樣品裝填方式
c. 不同膜排序方式
d. 不同樣品池
e. 不同流速的釋放曲線
圖 3 膜的典型排列方式
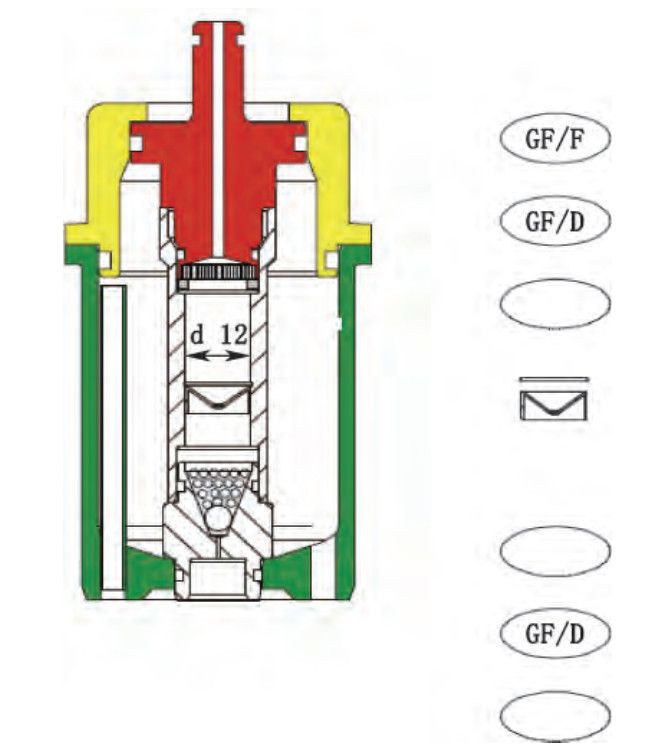
表 4 體外加速試驗(yàn)釋放度結(jié)果( mean±SD,%,n=6)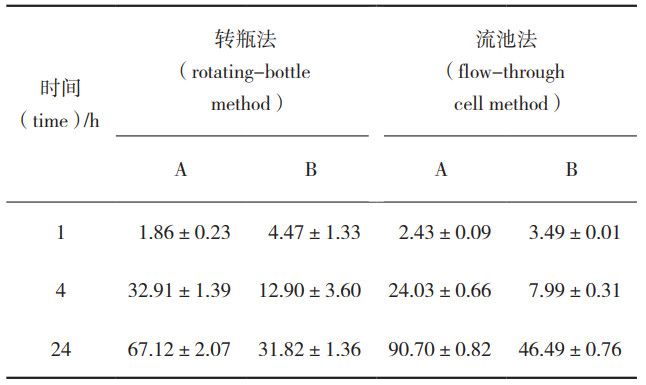
圖 4 A、B 組大鼠平均血漿奧曲肽濃度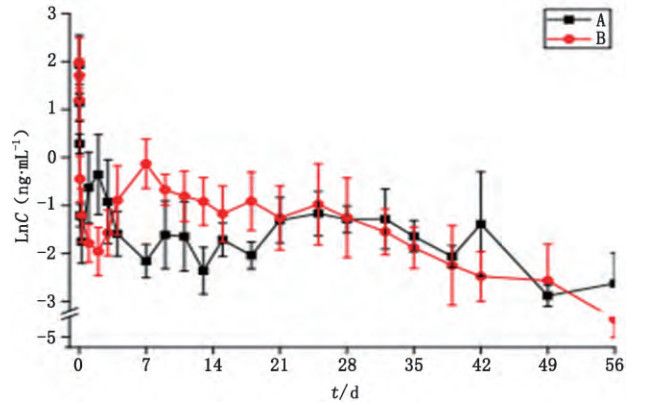
4.1 體外加速釋放測定方法
對比2種體外加速釋放測定方法,轉(zhuǎn)瓶法的操作更為簡單,但需注意取樣時勿粘取微球造成損失,導(dǎo)致釋放結(jié)果偏低;流通池法需要選擇合適的樣品池,避免微球溶脹,池內(nèi)壓力過大,導(dǎo)致釋放結(jié)果不準(zhǔn)確。 微球樣品在流池法條件下的釋放速率快于轉(zhuǎn)瓶法,針對釋放機(jī)制為擴(kuò)散和溶蝕作用的微球而言,流池法更為適合作為體外加速釋放的測定方法。
4.2 體內(nèi)釋放曲線和數(shù)學(xué)模型
將大鼠體內(nèi)釋放數(shù)據(jù)與流池法體外加速釋放數(shù)據(jù)利用Origin Pro 8.0軟件進(jìn)行相關(guān)性分析。根據(jù)D’SouzaS等。的研究,體內(nèi)釋放度可以利用曲線下面積的百分?jǐn)?shù)所表示,圖5為微球樣品 A、B 的體內(nèi)釋放曲線。
圖 5 樣品 A、B 的體內(nèi)釋放度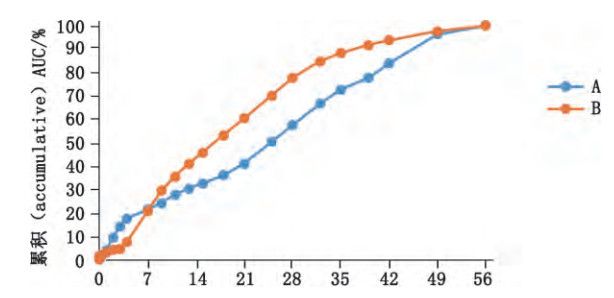
對體內(nèi)釋放數(shù)據(jù)利用Origin Pro 8.0 軟件中的Boltzmann、Logistic 等數(shù)學(xué)模型擬合曲線。Boltzmann方程:y=A2+(A1-A2 )/(1+exp(x-x0/dx))見圖6Boltzmann曲線;Logistic 方程:y=A2+(A1-A2 )/( 1+(x/x0 )p )見圖7Logistic曲線。
圖 6 Boltzmann 曲線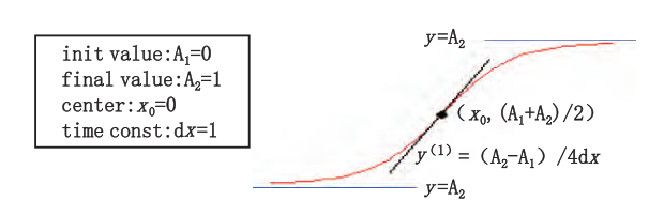
圖 7 Logistic 曲線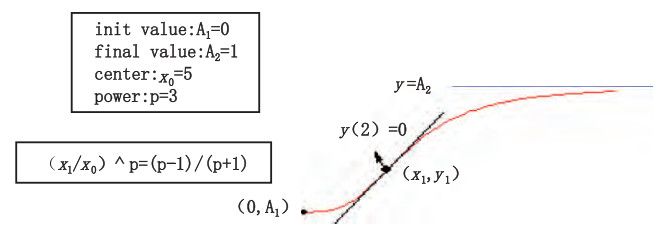
4.3 體內(nèi)外釋放度分析
本文結(jié)合體內(nèi)藥動學(xué)研究,對體內(nèi)與體外釋放數(shù)據(jù)進(jìn)行分析,探索體外加速釋放-體內(nèi)釋放的相關(guān)性。由表5和圖8-10可見,體外加速釋放(流池 法)線性擬合后,與將體內(nèi)釋放擬合曲線對應(yīng)的點(diǎn)利用最小二乘法進(jìn)行線性回歸。微球樣品 A、B體外加速釋放線性擬合曲線的決定系數(shù)r2分別為0.987 3、0.9275;對體外加速釋放-體內(nèi)釋放進(jìn)行線性回歸相關(guān)性分析,樣品A、B回歸直線的相關(guān)系數(shù)r分別為0.9982、0.9609。
結(jié)果表明,采用流池法測定體外加速釋放度,微球樣品A和樣品B的體外釋放與體內(nèi)釋放均具有良好的相關(guān)性。
本文以注射用醋酸奧曲肽微球?yàn)檠芯繉ο螅M(jìn)行了體外釋放度測定方法研究和體內(nèi)外釋放相關(guān)性初步研究。通過體外加速釋放試驗(yàn)方法研究,探索了影響奧曲肽微球釋放的因素,如溫度、pH、轉(zhuǎn)速、流速、樣品池的種類、膜的排列方式、玻璃珠以及樣品裝填方式等。建立了流池法測定奧曲肽微球制劑的釋放度,并比較了與轉(zhuǎn)瓶法的適用性。通過體內(nèi)外釋放相關(guān)性的探索性研究,建立了體內(nèi)釋放、體外加速釋放的擬合曲線,結(jié)果表明體外加速釋放與體內(nèi)釋放呈線性相關(guān)。本文建立的體外加速釋放流通池測定方法對于不同微球樣品有較好的區(qū)分力和良好的體內(nèi)外線性相關(guān),可用于注射液醋酸奧曲肽微球的質(zhì)量控制,與FDA推薦的PLGA緩釋微球體外釋放分析策
圖8 不同數(shù)學(xué)模型的樣品體內(nèi)吸收擬合曲線
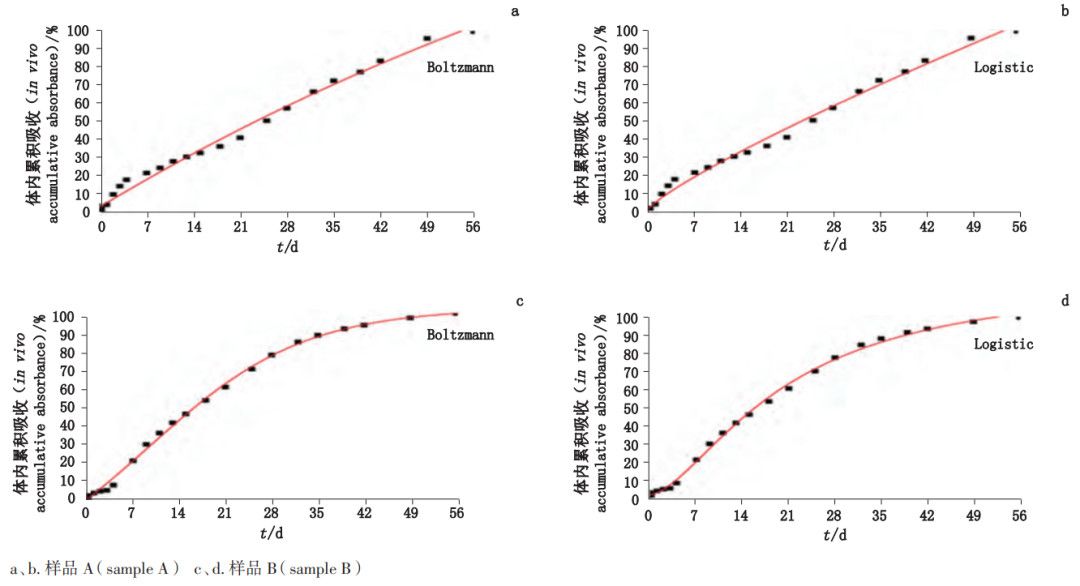 a、b. 樣品 A c、d. 樣品 B
a、b. 樣品 A c、d. 樣品 B
表 5 體內(nèi)釋放 - 體外加速釋放相關(guān)性分析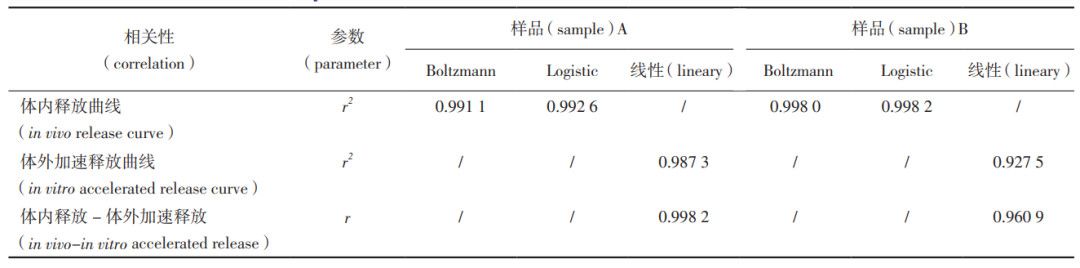
圖 9 樣品 A( a )、B( b )體外加速釋放曲線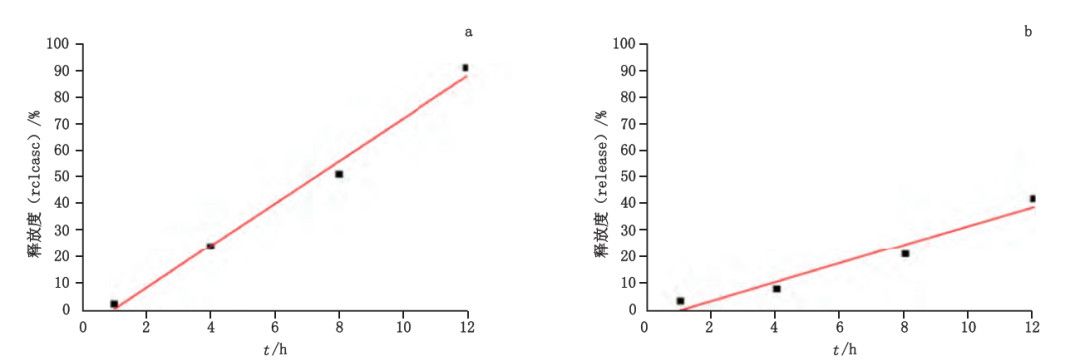
圖 10 樣品 A、B體內(nèi) - 體外加速釋放相關(guān)性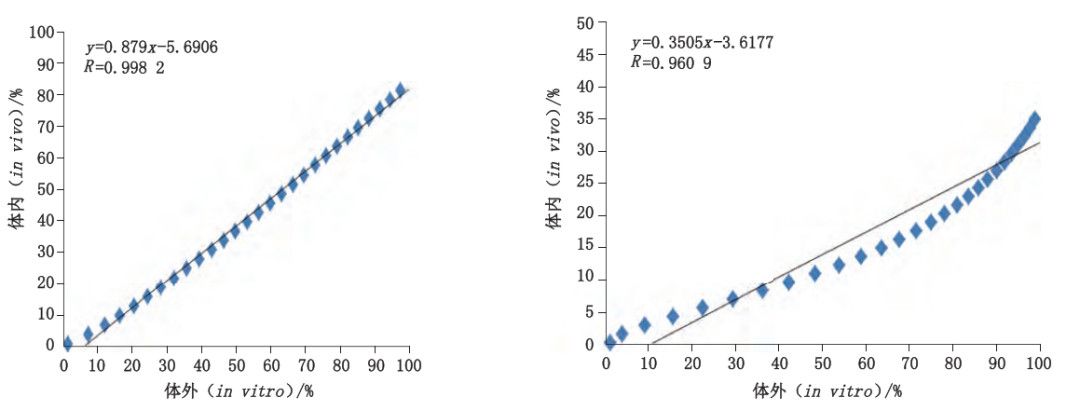
略一致,本研究為評價奧曲肽微球制劑的體外釋放度提供了新的測定方法,為深入開展肽類緩釋注射劑體內(nèi)藥代參數(shù)的預(yù)測研究積累了技術(shù)數(shù)據(jù)。
略
如需原文,請聯(lián)系小編(代老師15012941165)