時間:

目的:建立流通池測定曲安奈德益康唑乳膏兩個活性成分的釋放度方法。
方法:采用流通池法閉合系統裝置測定曲安奈德益康唑乳膏的釋放度,分別考察釋放介質、放置方式、流速及半透膜孔徑對兩個活性成分體外釋放曲線的影響,比較兩個生產企業市售產品體外釋放行為的差異;以HPLC測定釋放量,采用Luna C8柱(250 mm×4.6 mm,5 μm),梯度洗脫,檢測波長227 nm,柱溫40℃,流速1.0 mL/min,進樣量100 μL。
結果:以含0.05%十二烷基硫酸鈉的0.9%氯化鈉溶液為釋放介質,溫度為(32±0.5)℃,流速為16 mL/min,半固體適配器半透膜孔徑為2.7 μm,過濾裝置為0.45 μm混合纖維素膜,可以獲得既能有效釋放又具有一定區分力的釋放曲線。曲安奈德在濃度0.0052~0.7803 μg/mL范圍內線性良好(r=0.9994),硝酸益康唑在濃度0.0552~8.2851 μg/mL范圍內線性良好(r=0.9993)。兩個生產企業的體外釋放曲線存在顯著性差異,活性成分粒度可能是影響釋放行為差異的主要因素之一。

藥品審評中心(CDE)于2021年3月發布了《皮膚外用化學仿制藥研究技術指導原則(試行)》,指出對于處方組成復雜的軟膏劑、乳膏劑及凝膠劑等半固體制劑,由于具有多相、熱力學不穩定等特點,體外釋放的程度和速度將影響制劑質量與性能差異,應開展體外釋放試驗,但國內體外釋放試驗條件及操作方法仍缺乏明確的指導原則,其中指出建議參考國內、外相關文獻與指導原則開展相關研究工作。美國藥典2021版通則<1724>提供了半固體制劑體外釋放測定裝置,包括垂直擴散池(vertical diffusion cell, VDC)和流通池法(flow-through cell)。Chattaraj等早在1996年提出流通池法可用于半固體制劑體外釋放度研究,與垂直擴散池比較,流通池法更具有區分力且可以避免氣泡對測定結果的影響。流通池法早已經被國外多國藥典收載,《中國藥典》2020年四部新增第六法流池法,國內最近有文獻報道流通池法為貼劑、半固體制劑等特殊制劑的體外釋放度控制提供一種新的評價方法,但目前應用不多且方法不成熟。
曲安奈德益康唑乳膏是由Janssen公司開發的復方乳膏劑,規格為每克含硝酸益康唑10 mg與曲安奈德1mg,上市國家為英國、法國,商品名Pevaryl?/Pevisone?,原研未進口銷售,國內有16家生產企業。前期研究結果表明,地產化產品(商品名:派瑞松?)、國內仿制代表產品(商品名:邦力?)與原研產品的處方組成(Q1)、處方用量(Q2)、微觀結構特性(Q3)均存在較大差異。李震等采用垂直擴散池研究了不同廠家曲安奈德益康唑乳膏的體外透皮吸收試驗,但流通池法測定本品體外釋放度暫無報道研究。本文旨在建立流通池法測定體外釋放度方法,從而研究Q3對體外釋放行為差異的影響,以用于指導本品一致性評價研究,為豁免生物等效性研究提供研究依據。
2.1試驗儀器
流通池(推薦使用華溶DS-7CP流池法溶出系統);Thermo UltiMate 3000高效液相色譜儀(美國賽默飛公司);XP 205十 萬分之一電子天平(梅特勒-托利多公司)。
2.2藥品與試劑
曲安奈德益康唑乳膏(商品名派瑞松?,批號JKJOD80)購自A廠;曲安奈德益康唑乳膏(商品名邦力?,批號2019010)購自B廠;曲安奈德對照品(批號100055-201804)、硝酸益康唑對照品(批號100214-202005)購自中國食品藥品檢定研究院,質量分數均>98%;己烷磺酸鈉購自百塞勤化學技術有限公司;磷酸、四氫呋喃和四丁基氫氧化銨購自成都市科隆化學品有限公司;色譜級乙腈、異丙醇和甲醇購自安徽時聯特種溶劑股份有限公司。
3.1.1?色譜條件
辛烷基硅烷鍵合硅膠為填充劑(Luna C8,250 mm ×4.6 mm,5 μm),以取己烷磺酸鈉0.94 g,加乙腈-異丙醇-水-85%磷酸(140:140:720:1)溶解并稀釋至1000 mL為流動相A,以取己烷磺酸鈉0.94 g,加甲醇-水-85%磷酸(900:100:1)溶解并稀釋至1000 mL為流動相B,按表1梯度洗脫;檢測波長227 nm;柱溫40℃;流速1.0 mL/min;進樣量100 μL。
3.1.2 釋放條件
照溶出度與釋放度測定法(《中國藥典》2020年版四部通則0931第六法)測定。采用流通池法閉合系統裝置(釋放度試驗用流通池見圖1),取本品約0.1 g,均勻涂抹于孔徑為2.7 μm的半透膜,并置于半固體適配器(規格1.2 mL),放入內徑為22.6 mm的標準片劑池(半透膜朝下),以200 mL含0.05%十二烷基硫酸鈉的0.9%氯化鈉溶液為釋放介質,溫度為(32±0.5)℃,流速為16 mL/min,脈沖為120,經0、2、4、8、12、18、24和30 h取樣1.5 mL。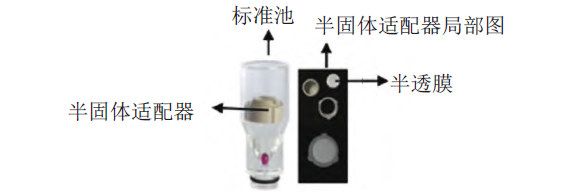
3.1.3?溶液的配制
取“3.1.2”項下釋放溶液作為供試品溶液。精密稱取曲安奈德對照品約10mg,置10mL量瓶中,用甲醇溶解并稀釋至刻度,作為曲安奈德對照品貯備溶液;另取硝酸益康唑對照品約10mg,置20mL量瓶中,精密加入曲安奈德對照品貯備溶液1mL,用甲醇溶解并稀釋至刻度,搖勻;精密量取1mL,置100mL量瓶中,用釋放介質稀釋至刻度,搖勻,作為對照品溶液。
3.2 體外釋放度方法學驗證
3.2.1?專屬性試驗
取本品約0.1 g,照“2.1.2”項下操作,經30 h取樣1.5 mL,作為供試品溶液。另取曲安奈德對照品與硝酸益康唑對照品各適量,照“2.1.3”項下配制對照品溶液。取上述溶液,按“2.1.1”項下色譜條件測定,記錄色譜(圖2)。結果表明,在本色譜條件下,曲安奈德、硝酸益康唑與相鄰色譜峰分離良好,溶劑峰不干擾測定。
3.2.2?精密度試驗
取對照品溶液100 μL,按“2.1.1”項下色譜條件連續進樣6針,記錄色譜圖,計算2個主成分峰面積相對標準偏差,結果曲安奈德與硝酸益康唑峰面積RSD分別為0.5%和0.2%,精密度良好。
3.2.3?線性關系考察
取曲安奈德與硝酸益康唑對照品各適量,用甲醇適量使溶解,加釋放介質稀釋制成系列對照品溶液,按“2.1.1”項下色譜條件測定,記錄色譜圖。以濃度(C)為橫坐標,峰面積(A)為縱坐標繪制標準曲線,計算回歸方程及相關系數。結果表明:曲安奈德在濃度0.0052~0.7803 μg/mL范圍內線性良好,回歸方程A=2.3944C+0.0167,相關系數0.9994;硝酸益康唑在濃度0.0552~8.2851 μg/mL范圍內線性良好,回歸方程A=4.1645C+0.1606,相關系數0.9993。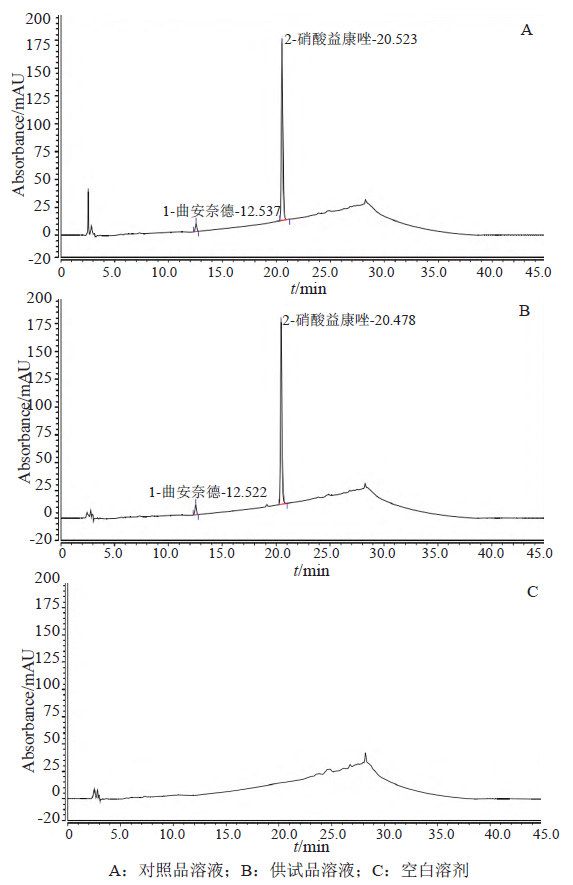
3.2.4?回收率試驗
取本品約0.05g,精密稱定,置200mL量瓶中,平行9份。另取對照品各適量,精密稱定,用適量甲醇溶解后,用釋放介質定量稀釋制成每1 mL中約含曲安奈德10 μg和硝酸益康唑100 μg的混合溶液,作為對照品貯備溶液。精密量取對照品貯備溶液4、5和7 mL各3份,分別置上述9個量瓶中,用釋放介質稀釋至刻度,搖勻,用0.45 μm濾膜濾過,取續濾液分別作為80%、100%和140%回收供試品溶液。取本品約0.1 g,置200 mL量瓶中,加甲醇適量超聲使溶解,用釋放介質稀釋至刻度,搖勻,用0.45 μm濾膜濾過,取續濾液作為供試品溶液。按“2.1.1”項下色譜條件測定,記錄色譜圖,并計算回收率。結果表明,曲安奈德和硝酸益康唑平均回收率分別為99.7%和99.8%,RSD分別為1.4%和1.1%(n=9)。
3.2.5?溶液穩定性
取本品約0.1 g,照“2.1.2”項下操作,經30 h取樣1.5 mL,作為供試品溶液。按“2.1.1”項下色譜條件測定,分別于0、8、12、24和72 h注入液相色譜儀,記錄色譜圖。計算兩個主成分峰面積相對標準偏差,結果表明,曲安奈德與硝酸益康唑峰面積RSD分別為0.3%和0.5%,說明在72 h內溶液穩定性良好。
3.2.6?溶液穩定性
取“2.2.3”項下溶液,逐級稀釋后注入液相色譜儀,依法測定,記錄色譜圖。以信噪比S/N=3:1計算檢測限,以信噪比為S/N=10:1計算定量限。檢測限為:曲安奈德 0.94 ng/mL、硝酸益康唑0.45 ng/mL;定量限為:曲安奈德 3.15 ng/mL、硝酸益康唑1.50 ng/mL。
3.3 釋放度測定條件的確定
3.3.1?釋放介質的選擇
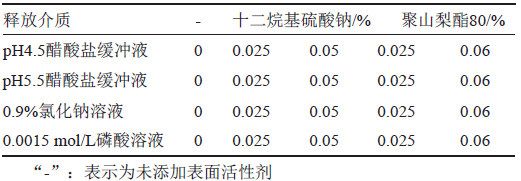
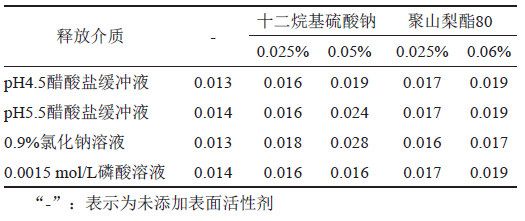
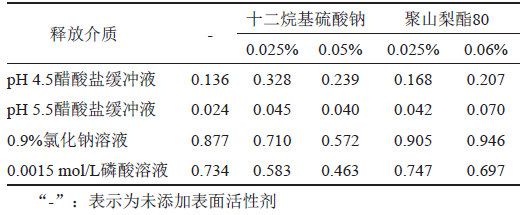
本品的給藥方式為皮膚局部用藥,皮膚的pH值大約在5.0左右,呈弱酸性,故本研究選擇pH 4.5醋酸鹽緩沖液、pH 5.5醋酸鹽緩沖液、0.0015 mol/L磷酸溶液及0.9%氯化鈉溶液共4種溶液,考察曲安奈德與硝酸益康唑在不含表面活性劑、含表面活性劑的釋放介質中的溶解度。取曲安奈德約10 mg和硝酸益康唑約20 mg,精密稱定,分別加入10 mL釋放介質(表2),溫度為25℃,以200 r/min持續攪拌24 h,取出,冷卻至室溫,離心,取上清液,按“2.1.1”項下色譜條件測定,記錄色譜圖,并計算溶解度。本品的規格為每1 g中含曲安奈德1 mg與硝酸益康唑10 mg,結果表明(表3~4),曲安奈德在含0.05%十二烷基硫酸鈉的0.9%氯化鈉溶液中溶解度最高;硝酸益康唑在0.9%氯化鈉溶液中的飽和溶解度明顯高于另3種介質。根據本品用法用量,每日早晚各給藥1次,結合前期不同給藥劑量的釋放曲線研究結果, 兩種活性成分釋放時間太長,不利于縮短評價時間,綜上所述,初步選擇含0.05%十二烷基硫酸鈉的0.9%氯化鈉溶液作為釋放介質。
3.3.2?放置方式的選擇
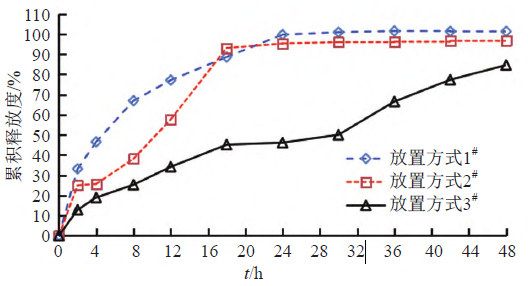
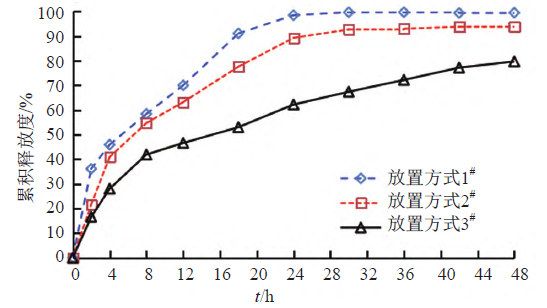
照溶出度與釋放度測定法(《中國藥典》2020年版四部通則0931第六法)測定。采用流通池法閉合系統裝置,取本品約0.1 g,載樣方式見表5,以200 mL含0.05%十二烷基硫酸鈉的0.9%氯化鈉溶液為釋放介質,溫度為(32±0.5)℃,活塞泵流速為8 mL/min,脈沖為120。分別經0、2、4、8、12、18、24、30、36、42和48 h取樣1.5 mL,取溶液按“2.1.1”項下色譜條件測定,記錄色譜圖,計算釋放量,繪制釋放曲線,研究載樣方式對釋放度的影響,結果見圖4~5。結果表明,雖然半固體適配器載樣方式的釋放慢于標準池直接載樣,但RSD值更小,重復性更好,故初步確定半固體適配器作為釋放度測定的載樣方式。
3.3.3?流速的選擇
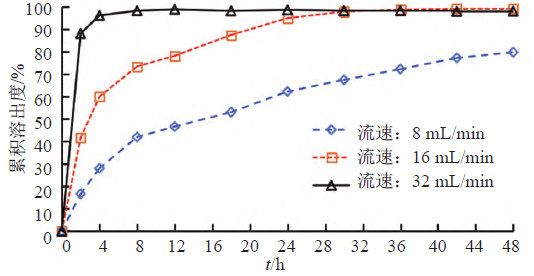
照溶出度與釋放度測定法(《中國藥典》2020年版四部通則0931第六法)測定。采用流通池法閉合系統裝置,取本品約0.1 g,均勻涂抹于玻璃纖維膜(孔徑2.7 μm),并置于半固體適配器(規格1.2 mL),放入內徑為22.6 mm的標準片劑池(膜朝下),以200 mL含0.05%十二烷基硫酸鈉的0.9%氯化鈉溶液為釋放介質,溫度為(32±0.5)℃,脈沖為120,分別以活塞泵流速為8、16和32 mL/min測定。經0、2、4、8、12、18、24、30、36、42和48 h取樣1.5 mL,取溶液按“2.1.1”項下色譜條件測定,記錄色譜圖,計算釋放量,繪制釋放曲線,研究流速對釋放度的影響,結果見圖6~7。結果表明,隨著流速的增加,在相同時間內藥物釋放量均顯著性增加,當流速為8 mL/min時,在48 h內兩個活性成分均不能達到釋放平臺;當流速為32 mL/min時釋放較快,只有2個點釋放度低于85%;16 mL/min有4個點釋放度低于85%。為更好計算釋放曲線相似因子,以評價不同產品體外釋放曲線差異,因此本研究選擇流速為16 mL/min,建立更具有區分力的體外釋放度方法。

3.3.4 半透膜孔徑的選擇
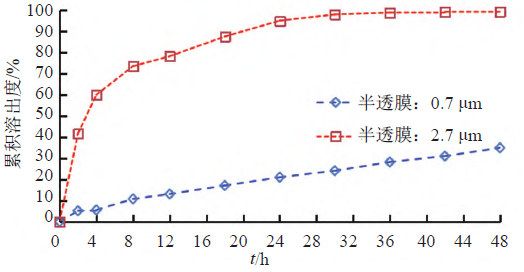
照溶出度與釋放度測定法(《中國藥典》2020年版四部通則0931第六法)測定。采用流通池法閉合系統裝置,取本品約0.1 g,分別均勻涂抹于孔徑為0.7和2.7 μm半透膜,并置于半固體適配器(規格1.2 mL),放入內徑為22.6 mm的標準片劑池(膜朝下),以200 mL含0.05%十二烷基硫酸鈉的0.9%氯化鈉溶液為釋放介質,溫度為(32±0.5)℃,脈沖為120,流速為16 mL/min。分別經0、2、4、8、12、18、24、30、36、42和48 h取樣1.5 mL,取溶液按“2.1.1”項下色譜條件測定,記錄色譜圖,計算釋放量,繪制釋放曲線,研究玻璃纖維膜孔徑對釋放度的影響,結果見圖8~9。結果表明,半固體適配器半透膜的孔徑大小對本品釋放速度影響較大,膜孔徑較小時,活性成分不能有效釋放,因此確定半透膜孔徑為2.7 μm。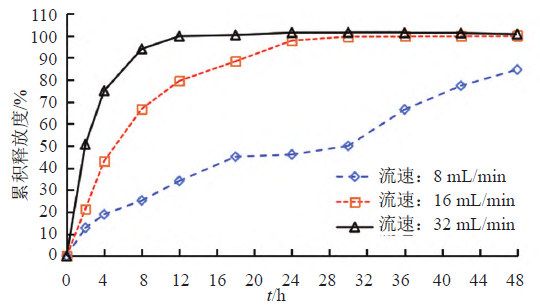

3.4 體外釋放度測定
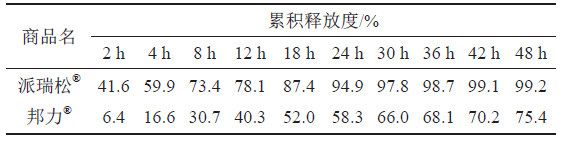
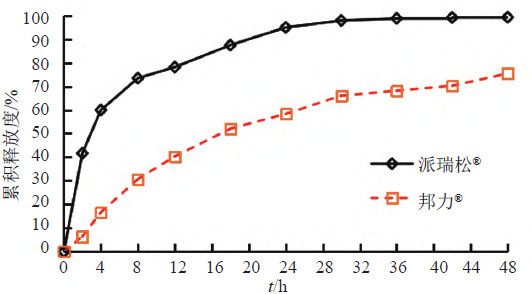
取A和B 兩個生產企業樣品各約0 . 1 g , 按“3.1.2”項下測定,分別經0、2、4、8、12、18、24、30、36、42和48 h取樣1.5 mL,取溶液按“3.1.1”項下色譜條件測定,記錄色譜圖,計算釋放量,繪制釋放曲線,比較2個不同廠家體外釋放曲線差異,結果見表6~7和圖10~11。結果表明,邦力?與派瑞松?的兩個活性成分溶出曲線均存在顯著性差異。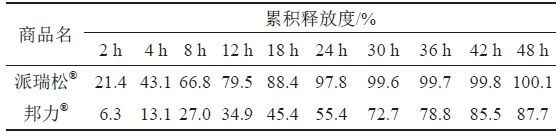
4.1 色譜條件的選擇
本研究參照《中國藥典》2020年版二部曲安奈德益康唑乳膏含量測定方法9,建立體外釋放度測定方法,由于本研究未能獲得兩個廠家的所有輔料,因此專屬性未能考察空白輔料溶液,但供試品溶液中兩個主峰峰純度角度均小于純度閾值,說明兩個主峰較純,輔料不干擾測定。本方法準確度好、靈敏度高,能夠準確檢測低濃度或高濃度水平,具有評價兩個主成分釋放速率變化的能力。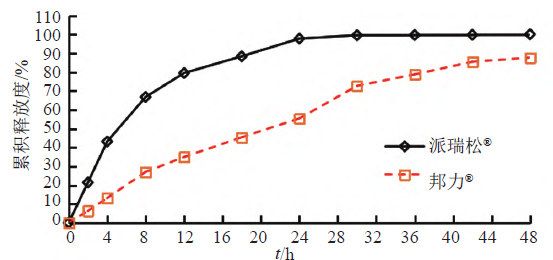
4.2 釋放介質的選擇
由于曲安奈德和硝酸益康唑均在水中極微溶解,必須選擇合適的介質同時滿足兩種活性成分的漏槽條件。李震等8采用0.9%氯化鈉注射液-無水乙醇(50:50,V/V)作為接受液,以Franz擴散池考察本品體外透皮吸收量,測定值顯著性高于0.9%氯化鈉注射液。由于本研究SOTAX流通池溶出儀未配置耐受有機相的標準池,故釋放介質考察時加入了表面活性劑,并對表面活性劑的種類和濃度進行考察,以增加藥物在介質中的溶解度,結果表明,選擇含0.05%十二烷基硫酸鈉的0.9%氯化鈉溶液作為釋放介質,對兩個活性成分均能滿足漏漕條件,采用閉合裝置系統可滿足測定要求,避免了開環裝置介質需求量大的缺點。
4.3 放置方式的選擇
流池法根據制劑特點配有相應的樣品池,包括標準片劑池(內徑分別為12 mm和22.6 mm)、半固體適配器、植入劑池等,對于半固體制劑,常用的放置方式有標準片劑池和半固體適配器。本研究考察了3種放置方式,結果表明:①標準片劑池底部加加玻璃珠的放置方式,玻璃珠能使溶媒形成層流狀態,故釋放更溫和。②標準片劑池中加入半固體適配器的放置方式,藥物需要從半固體適配器的玻璃纖維膜穿透,然后再溶解于釋放介質中,因此釋放最慢。本研究確定半固體適配器作為釋放度測定的放置方式,避免因樣品位置和高度差異引起RSD大的問題。
4.4 流速的選擇
流池法中流速是影響藥物溶出行為的重要參數,各國藥典標準流速為4、8和16 mL/min,目前經常使用的是16 mL/min。本研究通過對不同流速的考察,以確定具有一定區分力的釋放度條件。結果表明,在相同釋放時間內,釋放量隨著流速的增大而增大,最終確定流速為16 mL/min,既能滿足在一定時間內兩種活性成分均有效釋放,同時又具備區分力。
4.5 過濾裝置濾膜的選擇
另外,流通池還配置了一個過濾裝置,以獲得澄清的樣品溶液,從而進行含量測定,但是所用的濾膜應是惰性,不能明顯吸附溶液中有效成分。本研究分別以0.45 μm混合纖維素膜和0.45 μm尼龍濾膜考察釋放行為,結果表明,采用0.45 μm尼龍濾膜時,硝酸益康唑48 h累積釋放量約為80%,不能有效釋放,因此確定過濾裝置為0.45 μm混合纖維素膜。
4.6 釋放行為差異的分析
本文2個生產企業體外釋放度結果表明,邦力?與派瑞松?的曲安奈德釋放曲線相比較,相似因子f2(選取10個點)為22.1,差異因子f1(選取10個點)為57.7,硝酸益康唑釋放曲線相比較,相似因子(f2)為20.4,差異因子(f1)為57.1,說明二者釋放曲線存在顯著性差異,派瑞松?兩個活性成分釋放明顯快于邦力?。經分析,邦力?與派瑞松?Q1、Q2和Q3均差異顯著,Q3結果表明,派瑞松?乳滴粒度(5.71 μm)雖然大于邦力?(2.55 μm),但是派瑞松?活性成分粒度(32.36 μm)顯著性小于邦力?(149.82 μm),說明活性物質粒度可能是影響釋放差異的主要因素之一。
本文作者對曲安奈德益康唑乳膏的釋放度檢查進行了初步研究,篩選出具有良好區分力的流通池法體外釋放試驗方法,可用于本品質量控制,并指導處方及工藝研究。前期研究結果表明,本品推薦采用Janssen-Cilag Limited在法國上市的Pevisone?作為一致性評價的參比制劑(reference listed drug, RLD),但本次研究未能獲得該參比制劑,故市售產品與RLD體外釋放行為的差異還有待后續研究,從而為國內生產企業該品種一致性評價提供數據支撐。