時間:

翻譯:華溶應用中心
審核:工業藥劑發燒友
長效注射(Long acting injectables,LAI)混懸液是一種復雜的腸外給藥制劑,能夠在幾天至幾個月內持續釋放藥物。所有不可預測的藥物釋放行為都可能導致嚴重的副作用。因此,了解這些產品的體內外特性以及體內外相關性(IVIVC)非常重要。美國FDA推薦了一些LAI混懸液的體外釋放測試方法。但釋放時間都?于兩天,考慮到其在體內的療效達幾周至幾個月,可能不適用于建立LAI的IVIVC。本研究以醋酸甲羥孕酮注射混懸液為參比藥物,制備了三種不同粒徑、成分相同的醋酸甲羥孕酮混懸液,建立了與體內釋放時間更相關的體外釋放測試方法。使用了USP2法(配置透析袋、浸沒池和自制適配器)和USP4(使用半固體適配器)四種不同方法。使用浸沒池法和半固體適配器的USP4法對所研究的LAI混懸液的區分力和重現性最好。
一、介紹
長效注射劑(LAIs)旨在幾周至幾個月內達到長效治療的藥物,如抗精神病藥、避孕藥、抗糖尿病藥和抗前列腺癌藥物。長效注射劑一般分為:油溶液、油混懸液、納米晶體混懸液、微球和植?劑。與傳統劑型相比,腸外注射LAIs有許多優勢:1)藥代動力學的表觀半衰期由吸收速率常數控制;2)劑量和血漿水平之間有可預測的相關性;3)可能簡立體內外相關性(IVIVCs);4)可減少血漿濃度的峰谷水平;5)降低了用藥負擔,提高了患者的依從性。腸外LAI混懸液的長效作用是通過給藥后難溶性藥物在注射部位的緩慢溶解和分配來實現的。LAI混懸液比聚合物控釋更有優勢,因為其可用最少的藥用輔料達到更高的載藥量。迄今為止,美國FDA(表1)已批準的LAI混懸液有6種用于治療精神分裂癥,2種用于避孕(FDA橙皮書)。這些市售LAI混懸液的劑型可分為三類:粉末混懸劑(阿立哌唑注射混懸劑和奧氮平)、納?混懸液(阿立哌唑月桂醇和1個月帕利培酮棕櫚酸酯)和微米混懸液(阿立哌唑十二烷酸酯、1個月帕利培酮棕櫚酸酯和醋酸甲羥孕酮注射液)。
因此,建立一種穩定可靠的體外釋放試驗方法來評估不同制劑的體外釋放特性至關重要。理想的體外釋放試驗方法可以更易建立IVIVC,從而減少臨床研究。表1列出了現有美國FDA推薦的LAI混懸液的溶出或釋放測試方法。LAI混懸液推薦使用槳法或流池法。溶出方法持續時間為45min至2880min(2天)。這些方法可能不適合建立IVIVC,因為在臨床周期從幾周到幾個月,體外釋放持續時間比產品的體內療效持續時間要短得多。美國藥典推薦使用USP4用于USP通則<1092>以下的緩釋注射混懸液。但目前還沒有關于LAI混懸液釋放測試的指南或專著。理想情況下,一種體外釋放測試方法可用于多種目的,包括處方優化、產品質量控制和建立體內外相關性。為了在LAI混懸液中實現這一目標,必須開發更長持續時間釋放測試的方法。
醋酸甲羥孕酮(MPA)是一種用于避孕的皮下注射劑,每三個月注射一次,于2004年獲得美國FDA批準。該產品沒有USP或FDA推薦的釋放測試方法。在本研究中,選擇RLD醋酸甲羥孕酮(MPA)皮下注射劑作為參比藥物進行測試。如前所述,制備了定性和定量(Q1/Q2)等效的MPA混懸液(與RLD的組成和濃度相同)。藥物粒徑是研發LAI混懸液的一個關鍵屬性,因為它可能會影響這些制劑的體內外特性。以RLD醋酸甲羥孕酮(MPA)皮下注射劑為參考,使用3種不同粒徑的Q1/Q2等效混懸液配方(F1,F2和F3)來研究粒徑對MPA混懸液藥物釋放的影響。為了建立一種靈敏度高、可靠且區分力強(即粒徑)的MPA-LAI混懸液的體外釋放測試方法,我們使用了兩種使用了USP2法和USP4法,并對其進行了部分修改和優化。
二、材料和方法
2.1 材料
醋酸甲羥孕酮(MPA,微粉化,USP級)、聚乙二醇(PEG)3350(NF-USP)、吐溫80(NF級)、甲硫氨酸(USP級)、對羥基苯甲酸甲酯(NF級)和對羥基苯甲酸丙酯(NF級)( Spectrum Chemical Manufacturing Corp. New Brunswick, NJ, USA)。一水合磷酸鈉和十二水合磷酸氫二鈉(Sigma MA,USA)。PVP K17 PF(BSFA,Germany)。氯化鈉和十二烷基硫酸鈉(SDS)( Sigma MO,USA)。除非另有說明,所有材料均為分析級。
2.2 醋酸甲羥孕酮HPLC分析方法
使用安捷倫1290 HPLC系統分析醋酸醋甲羥孕酮樣品,流動相為乙腈-水(65/35,v/v)混合物,流速為1.5mL/min,色譜柱為C18柱(Kinetex,250×4.6mm,5μm,Phenomenex),柱溫30℃,紫外檢測波長244 nm,進樣量為50μL。使用安捷倫OpenLAB CDS工作站進行分析。MPA的保留時間為5.4分鐘。標準曲線在0.2–5μg/ml和5–100μg/ml兩個范圍內均顯示出良好的線性(R2=1)。
2.3 Q1/Q2等效的MPA混懸液的制備與表征
如前所述,制備Q1/Q2等效MPA混懸液。根據RLD處方將原料藥分散到混懸介質中。在本研究中,制備了三種不同粒徑的MPA LAI混懸液,以評估粒徑對藥物釋放的影響。處方1(F1)使用的原料藥粒徑接近13μm。處方2(F2)使用更?的粒徑,將API從丙酮-水(1:1,水作為反溶劑)中重結晶制得。重結晶API的物理性質(例如熔點和焓)以及物理形態與初始API相同。處方3(F3)使用更小粒徑,用探頭超聲減?粒徑,將F1超聲5min(10%功率超聲10s,每個周期停止1s)制備F3。使用馬爾文 3000和Hydro MV(中等體積)自動分散裝置對所有制劑的顆粒大小進行了表征。將混懸液添加到分散裝置的腔室中于以1640rpm的速度下攪拌。記錄混懸液的粒徑(體積加權)和粒徑分布(D10,D50,D90)。所有測量均重復3次,數據以平均值±標準差表示。
2.4 體外釋放試驗方法的建立
2.4.1 配透析管的USP2法
使用300 mL小溶出杯并配備透析管USP2法進行MPA混懸液的體外釋放測試。將截留分子量(MWCO)為100 kD到1000 kD的1 mL Float-A-Lyzers G2透析裝置(纖維素膜)連接到取樣針上。按要求處理透析管,去除甘油添加劑并用去離子水沖洗。在釋放測試之前,將透析管于釋放介質中浸泡過夜。將100uL MPA混懸液(共16 mg MPA)與900uL pH7.4的磷酸鹽緩沖液(PBS)混合,并將這1 mL混合物裝入透析管中。在含1% w/v SDS的300 mL pH7.4的PBS(37士0.5 C)中進行釋放試驗。攪拌速度為100±1 rpm,每天抽取1 mL樣本,并補充等體積新鮮介質。每7天完全更換并補充新鮮介質。藥物在釋放介質中的溶解度為545.98μg/mL。裝有透析管的容器中應保持良好的漏槽條件。回收試驗應使用同一儀器,唯一的區別是將藥物溶液而不是混懸制劑加入透析管中。在設定的時間間隔取出1mL樣品,并補充1ml新鮮介質。使用0.22um尼龍注射過濾器過濾樣品。考慮采樣或更換介質過程中的藥物損耗,計算累積釋放量。所有實驗均重復3次。
2.4.2 配浸沒池的USP2法
使用帶浸沒池(接觸面積為4cm2)的USP2法和200 mL平底溶出杯進行MPA混懸液的釋放測試(圖2)。上樣量為50μL MPA混懸液(總MPA為8 mg)。用預先在介質中浸泡好的膜(Whatman,GF/D,2.7μm)蓋好樣品。浸沒池按要求組裝。介質為150 mL含1% w/v SDS的pH7.4PBS, 轉速120 rpm, 溫度37±0.5℃。每天取樣并補充等體積介質。樣品經0.22μm的過濾器過濾后再進行HPLC分析。所有實驗重復3次。
2.4.3 使用自制裝置的USP2法
使用自制裝置(接觸面積:3.14 cm2)的USP2法和1L溶出杯進行釋放測試(圖3)。通過滑動而不是旋扭來避免樣品移動。注入50μL的MPA混懸液并使用2.7um的膜覆蓋樣品室。將約束帽滑入隔室固定好膜。介質為500 mL 1% w/v SDS水溶液,轉速為100±1 rpm,溫度為37±0.5℃。每天取樣1mL并補充等體積介質。樣品經0.22μm的過濾器過濾后再經HPLC分析。所有實驗重復3次。
2.4.4 帶半固體適配器的USP4法
使用USP4法配半固體適配器(深度:1 mm)進行MPA混懸液的釋放測試(圖4)。即將50μL的MPA混懸液裝入半固體適配器中,放入流通池。采用兩種孔徑玻璃纖維濾膜(Whatman? GF/D(孔徑為2.7μm)和GF/F(孔徑為0.7μm))。釋放介質為500 mL 1% w/v SDS,溫度37±0.5℃。采用3種流速(2 mL/min、4 mL/min和8 mL/min)考察流速對藥物釋放曲線的影響。每天取樣并補充等體積介質。樣品經0.22μm的過濾器過濾后再進行HPLC分析。所有實驗重復3次。
USP2法,長時間的釋放實驗會有介質蒸發,但可以通過適當的方法來緩解。為了最大限度地減少介質蒸發,所有可能導致介質損失的開口都使用了墊圈、塞子和O形圈。標記每個溶杯的介質的高度,每天進行觀察,確保沒有顯著的介質損失。USP4法是一個封閉系統,實驗過程中沒有介質損失。藥物在釋放介質中是穩定無降解的。體外釋放試驗表明,終濃度與理論濃度吻合較好。在HPLC色譜中未觀察到降解峰。
2.5 統計分析
使用OriginPro 2017軟件(OriginLab Corporation)進行數據分析。數據以均數±標準差(SD)表示。
三、結果與討論
3.1 Q1/Q2等效的MPA混懸液的粒徑
為了解藥物粒徑對藥物釋放的影響,制備了3種不同粒徑的Q1/Q2等效MPA混懸制劑。RLD和制備的MPA混懸液的粒徑和粒徑分布如圖5所示。所述處方的平均粒徑遵循F3
3.2 不同方法進行MPA混懸液的體外釋放試驗
不能確定商品化的RLD的輔料來源和生產工藝。F1的組成和濃度與RLD相同,但粒徑小很多。體外釋放試驗方法應該能夠檢測RLD和F1之間的任何差異。所有的釋放度檢測均采用RLD和配方F1,以檢驗所建立的檢測方法的區分能力。介質的選擇取決于裝置的屬性和漏槽條件。為了使透析管合適地安裝,透析方法(2.4.1)使用了300mL介質。USP2浸沒池裝置(2.4.2),所使用的溶出杯為USP規定的200mL的小杯。由于浸沒池占有一定的體積,所以介質使用150mL。USP2自制適配器裝置(2.4.3),使用標準的1L溶杯,以便在必要時有更?的空間調整到更高的釋放量。USP4法,介質體積可以隨意設置。為使兩種方法保持相似的漏槽條件,介質和體積與USP2自制適配器裝置法一致。無論使用哪種方法與參數,釋放測試方法應能夠區分Q1/Q2兩制劑,且該方法應具有可接受的重現性。
3.2.1 使用透析管的USP2法
3.2.1.1 透析管的回收率
為確保透析管沒有藥物吸附問題,對其進行處理。將含1% w/v SDS的PBS的MPA藥物溶液裝入透析管。實驗參數的設置與體外釋放試驗相同,然后在規定的時間點取出樣品。MPA的回收率在24小時內幾乎達到100%,這表明MPA在透析管不存在吸附問題。
3.2.1.2 使用帶透析管的USP2法測定RLD和F1的釋放曲線
RLD和F1的釋放曲線如圖6所示。LAI混懸液的釋放持續時間超過100天,與其他LAI混懸液的體外釋放試驗相比,這個時間非常長。透析管的MWCO對制劑的釋放速度和區分能力都有影響。當使用100 kD MWCO的透析管時,RLD和F1的釋放曲線重疊(圖6A)。較高MWCO (1000 kD)的透析管具有較高的釋放率和更好的區分能力(圖6B)。然而,Float-ALyzer方法在區分RLD和F1時靈敏度較低,盡管具有較高MWCO (1000 kD)的Float-A-Lyzer方法略好。區分處方的靈敏度低可能是由于透析帶中不滿足漏槽條件所致。雖然這種方法缺乏區分力,但使用MWCO大于1000 kD的透析膜或孔徑較大的膜可能有有所改善。不幸的是,市售透析管最高MWCO為1000 kD。所以后面的研究中考慮了合適孔徑的膜過濾器。所有配方都在微米尺寸范圍內(參見圖5),只有可忽略不計的部分在亞微米尺寸(低于截止尺寸)。當使用更高的截留分子量時,藥物釋放更快,是藥物分子的擴散速度更快,而不是亞微米顆粒的存在。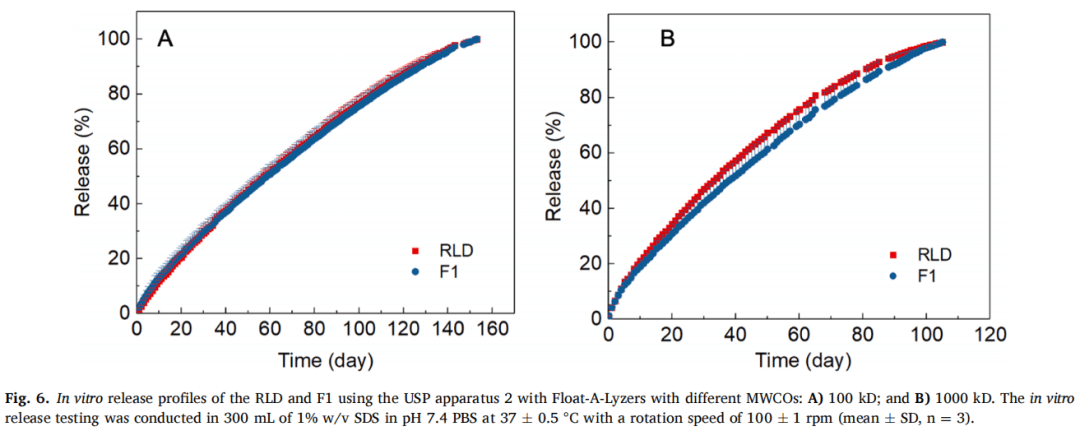
3.2.2 使用浸沒池裝置的USP2法
近期,USP2浸沒池裝置被用于軟膏和凝膠等半固體劑型。從透析法的結果來看,浸沒池可能是LAI混懸液釋放測試的一個可行選擇,因為使用USP2浸沒池裝置,市面上有比透析管孔徑更大的膜過濾器,RLD和F1的透析持續時間約為兩周,與透析法相比大大縮短。此外,該方法能夠區分RLD和F1(圖7)。該方法在除幾個早期時間點(第5天之前)外的所有時間間隔內均顯示出可接受的重現性(15%RSD)。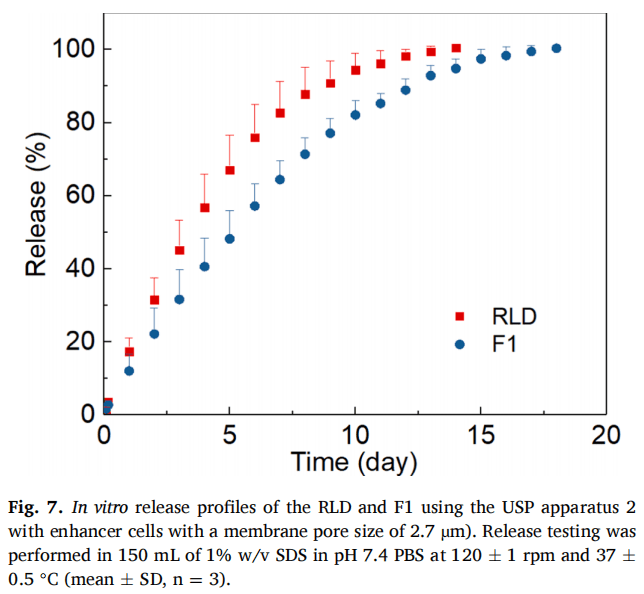
3.2.3 使用自制適配器的USP2法
為了使用USP2法的標準1 L溶出杯進行MPA混懸液的體外釋放測試,開發了一種適配器。這種適配器比浸沒池薄得多,且有不同帽的設計,浸沒池的固定帽需要擰緊,操作時可能會引起膜起褶皺。膜褶皺可能導致藥物泄漏或者與膜不完全接觸,造成結果重現性差。自制適配器的帽是通過滑動組裝的,這對膜和樣品的影響更少。兩種配方的釋放持續時間(~1個月)都比浸沒池法長(~2周)(圖8)。盡管誤差條很高,但使用自制適配器測定的RLD和F1的釋放曲線顯示出良好的區分力。與浸沒池法相比,RLD和F1的釋放曲線之間差值較大。然而,該裝置的缺點是釋放曲線變異較大,需要進一步的制造設計優化(正在進行中)。
3.2.4 使用半固體適配器的USP4儀器
USP4法儀器加半固體適配器首次被報告是測試眼部軟膏制劑(Xu et al.2015;Bao et al. 2017)。在本研究中,該方法也被用于混懸液的體外釋放測試,半固體適配器用來裝載樣品,適配器中不使用膜(圖9)。RLD和F1的釋放持續時間均約為1周。此方法對RLD和F1顯示出良好的區分力和重現性(小于5% RSD)。與USP2的浸沒池法和自制適配器法相比,USP4的半固體適配器法顯示出最好的重現性。這可能是因為USP4半固體適配器法中未使用膜,消除了膜對LAI混懸液樣品產生的誤差。USP2法中使用的膜(浸沒池或自制適配器)是為了便于裝樣,膜不會對藥物釋放產生擴散障礙或影響漏槽條件。但膜可能在組裝過程中起皺,或導致泄漏,從而引起誤差。
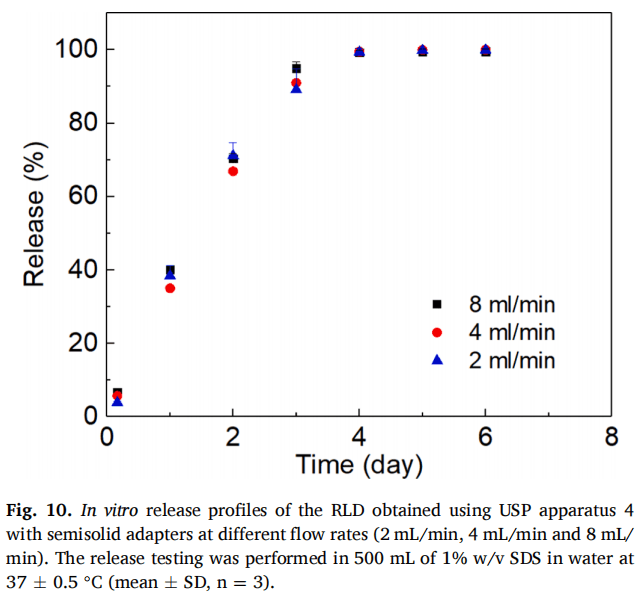
為了研究流速對釋放曲線的影響,以2mL/min、4mL/min和8 mL/min流速對RLD進行釋放測試(圖10)。不同流速下RLD的釋放曲線相互重疊,表明流速對LAI混懸液的藥物釋放曲線影響較?。另外,釋放曲線的誤差較小,證實了該方法具有良好重現性。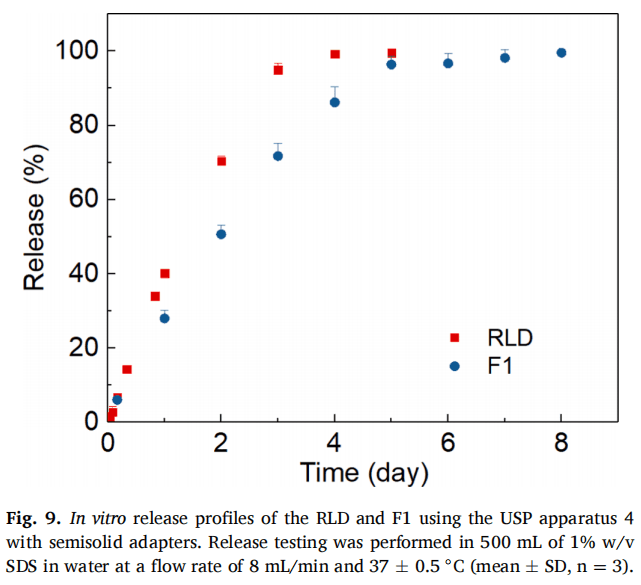
3.3 RLD和Q1/Q2等效MPA混懸液的釋放曲線
使用USP2浸沒池法(圖11A)、USP2自制適配器法(圖11B)和USP4半固體適配器法(圖11C)三種方法對RLD和三種Q1/Q2等效MPA混懸液進行釋放測試。三種方法均具有對不同粒徑的Q1/Q2等效MPA混懸液的區分能力。USP2自制適配器法對F1和F2的區分力較低。所有方法中,RLD和Q1/Q2等效MPA混懸液的釋放速率表現出相似的趨勢,順序依次為F3>RLD>F1>F2。由圖5可知,MPA混懸液的粒徑大小依次為F3
使用不同方法測試的MPA制劑的整體釋放特性表現出非常相似的趨勢和順序。所有方法的藥物釋放時間均有所延長,這是本研究所期望的。然而,使用不同的釋放試驗方法,藥物的釋放持續時間從大約1周到7周不等。這可能是由于三種方法之間介質的流體動力學差異所致。USP4半固體適配器法沒有使用膜覆蓋樣品,混懸液直接接觸釋放介質,所以藥物釋放速度更快或釋放時間更短。相反,在USP2的兩種方法(使用浸沒池或自制適配器)中,在混懸液的上方都加了玻璃纖維膜。薄膜本不應該成為藥物擴散的屏障,但混懸液處方中的藥物顆粒在浸沒池或自制適配器的腔體中保持不動,導致釋放速率變慢。兩種USP2法的藥物釋放率的差異在于:1)膜和裝置附近的流體動力學;浸沒池法中使用的小溶出杯和小槳,自制適配器法中使用的是1L標準溶出杯和槳;2)所用膜的接觸面積(浸沒池4 cm2,而自制適配器為3.14cm2);3)介質體積(浸沒池為150 mL,自制適配器為500 mL),所以漏槽條件不同;4)浸沒池和自制適配器樣品室的設計。
四、結論
本研究使用微小改動的藥典方法(USP2法和USP4法)進行了LAI混懸液的體外釋放測試。使用標準USP儀器可以在不同的實驗室進行比較。盡管使用透析管的USP2法釋放測試時間較長,但市售不同截留分子量(100 kD和1000 kD)的透析膜的區分能力都較差。USP2(使用浸沒池和自制適配器)和USP4(使用半固體適配器)法對不同粒徑的Q1/Q2等效LAI混懸液顯示出良好的區分能力,證實了藥物粒徑對LAI混懸液體外性能的影響(即粒徑越?釋放速率越快,反之亦然)。另外,USP4法結合半固體適配器的重現性最好,而USP2法對不同Q1/Q2等效MPA混懸液區分能力更好(誤差較大)。USP2法兩種裝置的釋放速率差異是由流體動力學、接觸面積、介質體積和樣品室設計等因素造成的。這些體外釋放測試方法的釋放持續時間較長,從一周到幾個月不等。所以可能更能反映LAIs的體內釋放情況,為IVIVCs的建立提供了一種有效的方法。
五、參考文獻
略
如需原文,請聯系小編(15012941165)