時(shí)間:

翻譯:華溶應(yīng)用中心
審核:工業(yè)藥劑發(fā)燒友
簡(jiǎn)介:
從歷史上看,為了證明生產(chǎn)工藝或輔料的變更對(duì)產(chǎn)品的質(zhì)量、療效和一致性的影響,需對(duì)半固體藥物產(chǎn)品進(jìn)行生物利用度/生物等效性研究,這類(lèi)研究工作一直具有挑戰(zhàn)性。體外測(cè)試如溶解度、粒徑、活性成分釋放率和產(chǎn)品均勻性的測(cè)定,已成為考察產(chǎn)品均勻性和質(zhì)量等效性的主要指標(biāo)。其中,活性成分的體外釋放試驗(yàn)(IVRT)因《非無(wú)菌半固體劑型工藝指南》(SUPAC-SS)的頒布而備受關(guān)注。
許多外用藥物制造商在藥物開(kāi)發(fā)過(guò)程中投入了大量資源來(lái)開(kāi)發(fā)和驗(yàn)證IVRT。然而,正如工廠檢驗(yàn)計(jì)劃意見(jiàn)書(shū)所指出的那樣,沒(méi)有一個(gè)標(biāo)準(zhǔn)的測(cè)試方案可以適用于所有半固體劑型。本研究采用Franz擴(kuò)散池對(duì)不同半固體制劑中的維甲酸進(jìn)行了釋放試驗(yàn),測(cè)試的產(chǎn)品是含有維甲酸的乳膏。使用維甲酸開(kāi)發(fā)并驗(yàn)證IVRT,然后將IVRT方法應(yīng)用于制劑開(kāi)發(fā),并證明工藝變更的影響。選擇維甲酸是因?yàn)樗休^多規(guī)格類(lèi)型可以提供研究,且前人對(duì)維甲酸乳膏中維甲酸的釋放研究比較充分。
1、試驗(yàn)方法:
雖然通常有一種測(cè)定方法可用于測(cè)定目標(biāo)原料藥及其相關(guān)化合物,但這種方法可能不適合原料藥在特定的接收介質(zhì)下進(jìn)行檢測(cè)。在大多數(shù)情況下,在選定的接收介質(zhì)中分析這些化合物時(shí),為了保證IVRT結(jié)果的可靠,需要對(duì)方法進(jìn)行一定程度的修改,并對(duì)修改后的方法進(jìn)行完整的驗(yàn)證。對(duì)測(cè)定方法進(jìn)行了修改,以測(cè)定含有30-35%乙醇的磷酸鹽緩沖液(pH 5.5)中的微量維甲酸,經(jīng)過(guò)實(shí)驗(yàn)30-35%乙醇被證明是維甲酸釋放的適當(dāng)有機(jī)相范圍。
2、膜的選擇:
所選擇的膜應(yīng)為試驗(yàn)試劑提供持續(xù)的惰性接觸表面,允許活性成分從劑型中釋放時(shí)容易擴(kuò)散到接收介質(zhì)中,而不能成為限速屏障。重要的是要確認(rèn)膜和制劑之間沒(méi)有物理或化學(xué)的相互作用。在許多情況下,制劑中存在的輔料可能影響膜的物理完整性,制劑的活性成分還可能與膜結(jié)合發(fā)生粘附,難以擴(kuò)散。此外,膜不應(yīng)含有任何可能干擾活性成分測(cè)定的可浸出物。在方法開(kāi)發(fā)之初,常用的膜有Tuffryn、聚醚砜樹(shù)脂、纖維素、醋酸纖維素、尼龍、特氟龍和聚碳酸酯。建議在IVRT實(shí)驗(yàn)預(yù)期的上限和下限濃度范圍內(nèi),選幾個(gè)濃度水平制備受試化合物在接收介質(zhì)中的標(biāo)準(zhǔn)溶液,用于驗(yàn)證藥物與膜的結(jié)合程度。用市售的過(guò)濾器將測(cè)試的膜裝好,將維甲酸標(biāo)準(zhǔn)溶液通過(guò)這些膜進(jìn)行過(guò)濾,并分析過(guò)濾后標(biāo)準(zhǔn)溶液中視黃酸的回收率。
對(duì)含維甲酸的制劑,參照文獻(xiàn)選取濃度為0.1、0.02 μg/ml的藥物進(jìn)行膜吸附檢測(cè)。在篩選的膜中,聚砜樹(shù)脂膜和Tuffryn膜在低水平(0.02 μg/ml)下對(duì)維甲酸有明顯吸附。高效液相色譜(HPLC)顯示,醋酸纖維素膜回收率最高,無(wú)正干擾(表1)。因此,選擇醋酸纖維素膜進(jìn)行進(jìn)一步的方法開(kāi)發(fā)和驗(yàn)證。
許多研究者建議用接收介質(zhì)或0.5%肉豆蔻酸異丙酯浸泡膜進(jìn)行預(yù)處理。然而,對(duì)于維甲酸乳膏,膜的預(yù)處理對(duì)總體釋放曲線幾乎沒(méi)有影響。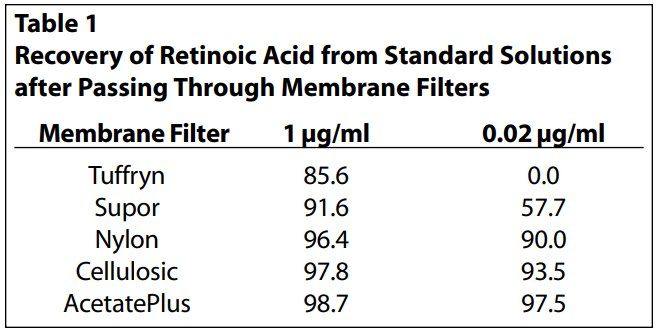
3、接收介質(zhì)選擇:
雖然希望接收介質(zhì)與皮膚的生理狀況相似,但也必須確保藥物有足夠的釋放可以無(wú)偏差地被測(cè)量,選擇接收介質(zhì)時(shí)最重要的因素是活性成分在介質(zhì)中的溶解度,接收介質(zhì)需要為活性成分從半固體制劑中釋放提供外部的擴(kuò)散條件。Q(累積釋放量)與√T(時(shí)間的平方根)的關(guān)系是從Higuchi模型推導(dǎo)出來(lái)的,該模型假設(shè)始終有藥物儲(chǔ)庫(kù)可用。根據(jù)經(jīng)驗(yàn),在實(shí)驗(yàn)結(jié)束時(shí),釋放到介質(zhì)中的劑量不應(yīng)超過(guò)所使用劑量總量的30%。
介質(zhì)的pH值也是一個(gè)需要考慮的重要因素。介質(zhì)的水性組分pH值應(yīng)基于制劑的pH值、活性成分的pH-溶解度曲線和目標(biāo)膜的pH值來(lái)選擇。對(duì)于接收介質(zhì),一個(gè)實(shí)際的考慮因素是選擇的接收介質(zhì)應(yīng)滿足在合適時(shí)間內(nèi)釋放足量活性成分,以確保準(zhǔn)確分析樣品釋放速率。
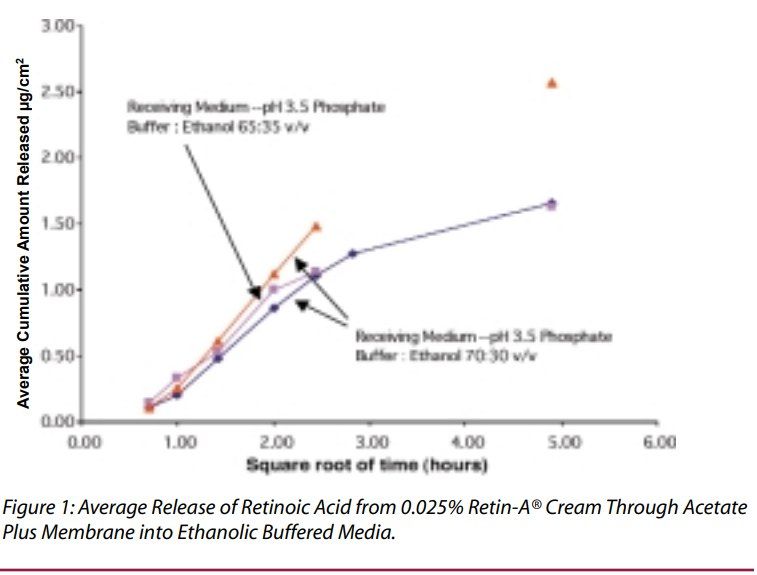
維甲酸在乙醇接收介質(zhì)中的溶解度足以滿足上述所有要求。經(jīng)過(guò)幾次初步實(shí)驗(yàn)后,選擇含有35%乙醇的pH3.5磷酸鹽緩沖液作為接收介質(zhì),該介質(zhì)允許足夠水平的維甲酸從制劑中釋放并通過(guò)膜擴(kuò)散,以準(zhǔn)確分析維甲酸釋放情況。使用pH3.5和pH5.5緩沖液(分別為受試制劑的pH和皮膚pH)對(duì)幾種試驗(yàn)用制劑進(jìn)行平行檢測(cè),0.025%維甲酸乳膏的釋放速率在pH 3.5緩沖液中較快,而某些原研制劑(8和9)在這兩種pH緩沖接收介質(zhì)中的釋放速率幾乎沒(méi)有差異(表2)。我們將pH5.5的緩沖液:乙醇(65:35 v/v)作為進(jìn)一步實(shí)驗(yàn)的接收介質(zhì)。乙醇濃度的小幅度變化不會(huì)導(dǎo)致維甲酸釋放率發(fā)生顯著變化。(圖1)。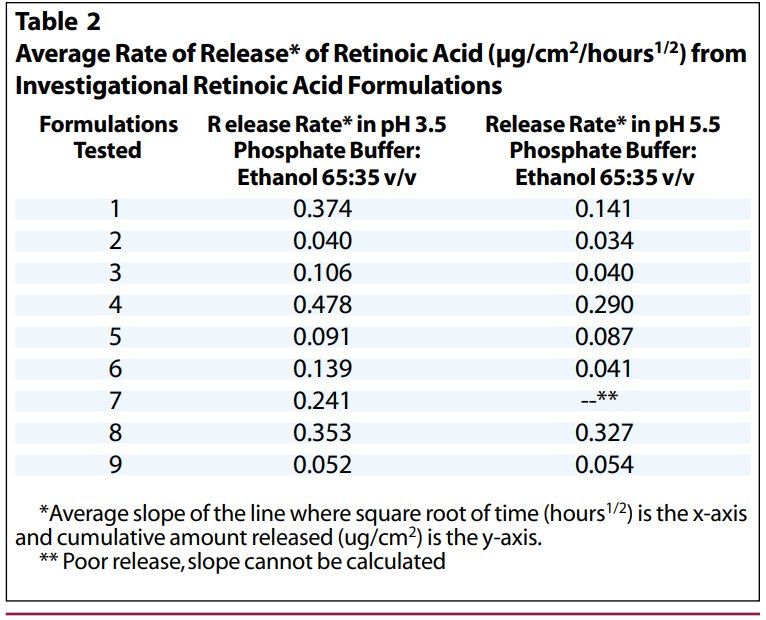
4、設(shè)備相關(guān)參數(shù)的選擇和藥物釋放度計(jì)算:
在進(jìn)行釋放試驗(yàn)時(shí)應(yīng)考慮以下具體的設(shè)備相關(guān)參數(shù)。儀器通常使用6個(gè)Franz擴(kuò)散池用于釋放試驗(yàn)(推薦使用華溶TD-12AT透皮擴(kuò)散系統(tǒng))。推薦使用華溶TD-12AT透皮擴(kuò)散系統(tǒng)試驗(yàn)溫度在大多數(shù)情況下,當(dāng)劑型應(yīng)用于皮膚時(shí),32℃是合適的。特殊情況是,當(dāng)劑型應(yīng)用于管腔膜,如陰道粘膜,在這種情況下,37℃更合適。我們本次研究所有的實(shí)驗(yàn)都使用32℃。
取樣時(shí)間點(diǎn)(h):0.5、1、2、4、6、8、24、48。
取樣體積:每個(gè)時(shí)間點(diǎn)取樣0.2ml,每次用新鮮介質(zhì)補(bǔ)液。
計(jì)算:維甲酸在膜單位表面積上的累積釋放量(Q)為:
n-1 Q= {CnV+∑CiS}/A i=1
其中
Q =膜單位面積維甲酸累積釋放量(μg/cm)
Cn =第n個(gè)采樣間隔測(cè)定的維甲酸濃度(μg/ml)
V =單個(gè)Franz擴(kuò)散池的體積
n-1 ∑Ci =在采樣間隔1到 n-1期間測(cè)定的維甲酸濃度之和(μg/ml)
i=1
S =取樣等分液的體積,0.2 m
A =樣品孔的表面積。本次實(shí)驗(yàn)表面積為1.767 cm2
通常,需要對(duì)具有已知差異的制劑進(jìn)行驗(yàn)證。在這種情況下,該方法首先使用已上市產(chǎn)品retin-A乳膏進(jìn)行驗(yàn)證,確認(rèn)方法的可行性,然后將驗(yàn)證后的方法應(yīng)用于具有已知差異的自制制劑,以確認(rèn)該方法對(duì)正在進(jìn)行工藝探索的不同制劑的區(qū)分能力。
驗(yàn)證的內(nèi)容
(1)、重現(xiàn)性:評(píng)價(jià)儀器的長(zhǎng)期穩(wěn)定性、方法的穩(wěn)定性、 操作對(duì)結(jié)果的影響等
(2)、準(zhǔn)確度:不同時(shí)間測(cè)試的同一制劑批次之間的一致性
(3)、劑量規(guī)格對(duì)釋放速率的影響
(4)、組成變化對(duì)釋放速率的影響
(5) 、工藝參數(shù)變化對(duì)釋放速率的影響
(6)、劑型粘度變化對(duì)釋放速率的影響
1、重現(xiàn)性: 評(píng)價(jià)儀器的長(zhǎng)期穩(wěn)定性、方法的穩(wěn)定性、 操作對(duì)結(jié)果的影響等
在沒(méi)有Franz擴(kuò)散池重現(xiàn)性考察標(biāo)準(zhǔn)品的情況下,使用內(nèi)部標(biāo)準(zhǔn)品Retin-A乳膏0.025%作為參比制劑。此外,還計(jì)算了樣品釋放時(shí)間平方根(x軸)和單位面積累計(jì)釋放量(y軸)所描述的直線的斜率和相關(guān)系數(shù)。相關(guān)系數(shù)< 0.98的直線不符合要求
2、 準(zhǔn)確度: 同一成分在不同時(shí)間測(cè)試的批次之間的“一致性”
若用具有相同成分和相同制備工藝的維甲酸乳膏在不同時(shí)期試驗(yàn),這些制劑應(yīng)有非常相似的釋放速率。表3顯示了一個(gè)示例。
3、計(jì)量對(duì)釋放速率的影響
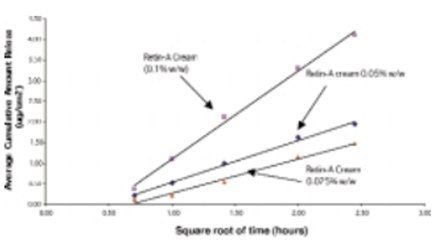
在上述條件下,測(cè)定了劑量規(guī)格為0.025%、0.05%和0.1%的維甲酸乳膏中維甲酸釋放情況 (上樣量都一致,但規(guī)格不同),評(píng)價(jià)規(guī)格對(duì)釋放速率的影響。圖2顯示了這些處方中維甲酸的釋放曲線。在pH 5.5磷酸鹽緩沖液:乙醇(65:35 v/v)溶液中維甲酸乳膏的藥物釋放速率和釋放總量成正比。圖3顯示了三批相同的自制維甲酸制劑的釋放曲線,兩批為0.025%,一批為0.05%。雖然初始釋放速度較慢,但與在維甲酸乳膏中觀察到的釋放量和釋放速度比值相同。因此,在試驗(yàn)的第一個(gè)小時(shí)后,釋放藥物的平均累積量與時(shí)間平方根之間存在線性相關(guān)性。
4、組成變化對(duì)釋放速率的影響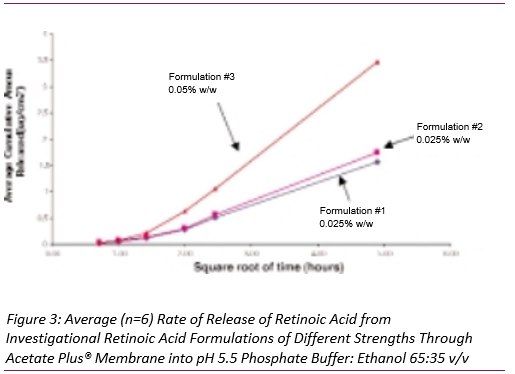
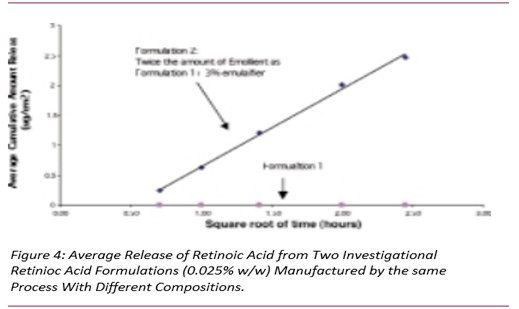
圖4顯示了兩種0.025%規(guī)格制劑中維甲酸的釋放。采用相同工藝生產(chǎn),制劑1幾乎未釋放出視黃酸,而制劑2釋放出大量維甲酸,制劑2含有兩倍量的潤(rùn)滑劑和其他調(diào)節(jié)劑。
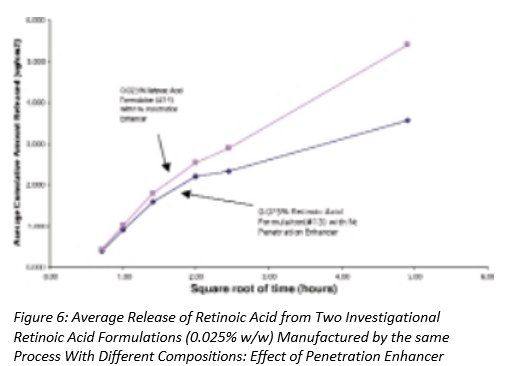
圖5-7顯示了三組自制制劑中維甲酸的釋放,其中制劑之間的唯一差異是是否存在滲透促進(jìn)劑。在圖5和圖6中,添加了該成分的維甲酸釋放量更高,而在圖7中,兩種制劑的釋放量沒(méi)有顯著差異。請(qǐng)注意,這些制劑的粘度存在差異,這可能會(huì)對(duì)藥物釋放產(chǎn)生影響。(見(jiàn)下面的討論)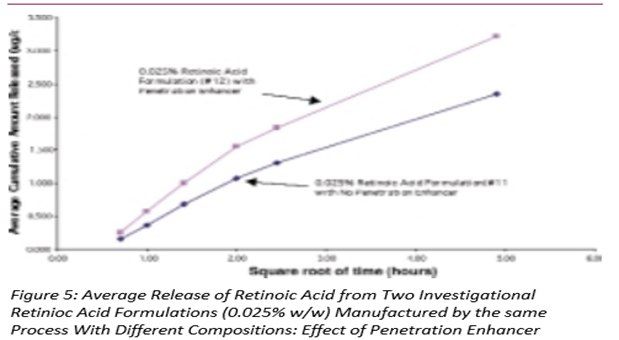
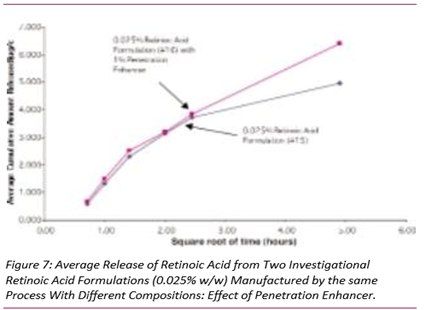
5、工藝參數(shù)變化對(duì)釋放速率的影響
表4顯示了維甲酸完全直接溶解在油相或者預(yù)溶于有機(jī)溶劑中的兩種制劑。當(dāng)藥物全部或部分預(yù)溶于有機(jī)溶劑時(shí),維甲酸的釋放量更大。從實(shí)驗(yàn)室規(guī)模擴(kuò)大到生產(chǎn)規(guī)模是一個(gè)必須評(píng)估的變量。對(duì)于劑型研究,批量從3KG擴(kuò)大至100 KG對(duì)自制制劑3的釋放率沒(méi)有影響,但對(duì)自制制劑2的釋放有顯著影響。表5顯示了不同規(guī)模生產(chǎn)的自制制劑的藥物釋放比較結(jié)果。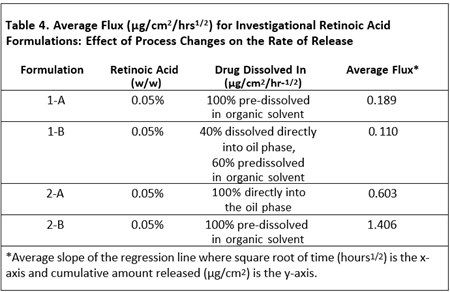
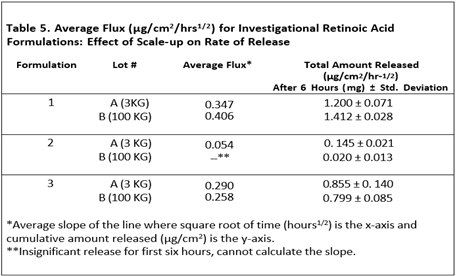
6、粘度變化對(duì)釋放速率的影響
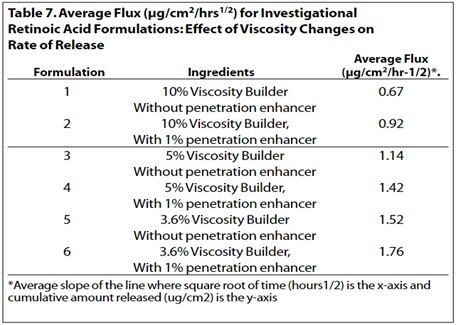
粘度是半固體劑量的關(guān)鍵屬性之一,觀察到粘度變化對(duì)維甲酸從原研制劑中釋放的有顯著影響。表6和表7顯示了黏度增強(qiáng)劑對(duì)這些處方中藥物釋放的影響。在表6中自制制劑1-4、5-7和8-11均顯示出相似的趨勢(shì),即維甲酸的釋放量與制劑中粘度度增強(qiáng)劑的量成反比。
在表7中,自制制劑1-6顯示了組分變化和粘度變化對(duì)維甲酸釋放的綜合影響。其對(duì)制劑組1-2和3-4之間的釋放曲線影響顯著,對(duì)制劑5和6之間的影響不太明顯 (見(jiàn)圖5-7)。然而,制劑1和2、3和4以及5和6均顯示出類(lèi)似的趨勢(shì),即藥物釋放與制劑中的粘度增強(qiáng)劑的量成反比。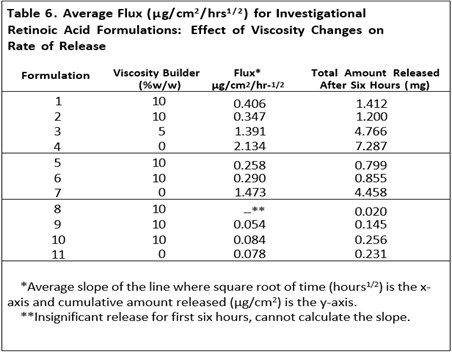
(1)、維甲酸的IVRT可以區(qū)分制劑的處方組成、生產(chǎn)工藝和粘度的變化。
(2)、本研究為維甲酸制劑開(kāi)發(fā)中IVRT提供了一種評(píng)估藥品質(zhì)量和SUPAC-SS要求的“一致性”的有用工具。
(3)、應(yīng)注意,IVRT僅對(duì)那些被測(cè)試的參數(shù)有
(4)、必須具體確定乙醇(在接收質(zhì)中)反擴(kuò)散對(duì)制劑的影響,以及每種方法變量“靈敏度”(最小鑒別濃度差異),作為完整方法驗(yàn)證的一部分。
略
如需原文,請(qǐng)聯(lián)系小編(15012941165)